题目内容
20. 水是人类宝贵的自然资源.
水是人类宝贵的自然资源.(1)天然水中含有许多杂质,实验室常用过滤方法除去水中不溶性杂质,过滤需要用到的仪器有带铁圈的铁架台、烧杯、漏斗和玻璃棒(填仪器名称).
(2)硬水给生活和生产带来很多麻烦,生活中常用煮沸的方法降低水的硬度.
(3)自来水生产过程中过常通入氯气等物质,其中氯气的作用是杀菌消毒.
(4)在电解水的实验中,两电极相连的玻璃管上方产生的气体是氧气和氢气,一段时间后,氧气和氢气的体积比约为1:2.
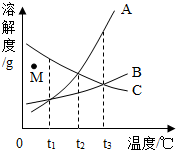
(5)如图为A、B、C三种固体物质的溶解度曲线图(A、B、C析出晶体时均不含结晶水),根据曲线图回答下列问题
①t1℃时,溶解度最大的物质是C.
②若将M点处C的不饱和溶液变为饱和溶液,可以选择的方法是BC(填序号).
A.降低温度 B.增加溶质 C.蒸发溶剂
③t2℃时,将等质量的A、B、C的饱和溶液都升温到t3℃,溶液中溶剂质量的大小关系是(忽略水的挥发)A=C<B.
分析 (1)考查过滤需要用到的仪器;
(2)考查降低水的硬度的方法,降低水的硬度的方法是:在生活中是加热煮沸,在实验室中是蒸馏;
(3)自来水生产过程中过常通入氯气等物质,其中氯气的作用是:杀菌消毒;
(4)考查电解水的实验;
(5)根据题目信息和溶解度曲线可知:A、B两种固体物质的溶解度,都是随温度升高而增大,而C的溶解度随温度的升高而减少;t1℃时,溶解度最大的物质是C,若将M点处C的不饱和溶液变为饱和溶液,可以选择的方法是:升高温度、增加溶质、蒸发溶剂;t2℃时,将等质量的A、B、C的饱和溶液都升温到t3℃,溶液中溶剂质量的大小关系是A=C<B,因为A和C在t2℃时的溶解度相等,因此水一样多,B的溶解度小,因此水最多,升温后水不变.
解答 解:(1)过滤需要用到的仪器有带铁圈的铁架台、烧杯、漏斗和玻璃棒;故答案为:玻璃棒;
(2)降低水的硬度的方法是:在生活中是加热煮沸,在实验室中是蒸馏;硬水给生活和生产带来很多麻烦,生活中常用煮沸的方法降低水的硬度;故答案为:煮沸;
(3)自来水生产过程中过常通入氯气等物质,其中氯气的作用是:杀菌消毒;故答案为:杀菌消毒;
(4)在电解水的实验中,两电极相连的玻璃管上方产生的气体是氧气和氢气,一段时间后,氧气和氢气的体积比约为1:2;故答案为:1:2;
(5)根据题目信息和溶解度曲线可知:A、B两种固体物质的溶解度,都是随温度升高而增大,而C的溶解度随温度的升高而减少;t1℃时,溶解度最大的物质是C,若将M点处C的不饱和溶液变为饱和溶液,可以选择的方法是:升高温度、增加溶质、蒸发溶剂;t2℃时,将等质量的A、B、C的饱和溶液都升温到t3℃,溶液中溶剂质量的大小关系是A=C<B,因为A和C在t2℃时的溶解度相等,因此水一样多,B的溶解度小,因此水最多,升温后水不变;故答案为:①C;②BC;③A=C<B;
点评 本考点考查了过滤、硬水和软水的区分、水的电解、溶解度曲线及其应用等,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

| A. | Na2SO4 CuSO4 | B. | CaCO3 Na2CO3 | C. | NaOH Na2CO3 | D. | NaCl Na2SO4 |
 探究皮蛋的奥秘
探究皮蛋的奥秘皮蛋也叫松花蛋,是人们喜爱的食品,加工皮蛋的原料是禽蛋和灰料,人们一般用水将灰料调成糊状,涂于新鲜的禽蛋上.密封保存一段时间后,即可得到皮蛋.查阅资料得知,皮蛋灰料的主要原料是生石灰、纯碱、食盐等.
小英和兴趣小组的同学对皮蛋灰料进行了研究.请你参与他们的探究,并回答有关问题:
(1)小组的同学取少量的灰料于烧杯中,加水充分搅拌后,过滤.此过程中发生了哪些化学反应?请写出有关反应的化学方程式:CaO+H2O═Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
(2)小组的同学对(1)得到的滤液的成分进行了探究:
【提出问题】滤液中的溶质是什么?
【做出猜想】
①小英对滤液中溶质的成分做出了三种猜想,请你帮她补充完整.
猜想一:氯化钠、氢氧化钠;猜想二:氯化钠、氢氧化钠、氢氧化钙;猜想三:氯化钠、氢氧化钠、碳酸钠.
【设计并实验】
②小英和小组同学一起设计并进行了实验,请将下表补充完整:
| 实验操作 | 实验现象 | 实验结论 |
| 结论:滤液呈碱性 | ||
| 结论:猜想2不成立 | ||
| 结论:猜想3成立 |
如何设计实验方案验证(1)得到的滤液放置一周后含有NaOH呢?小组的同学设计方案进一步探究,请填写如表:
| 实验操作 | 实验现象 | 实验结论 |
④根据上述探究过程,为了减轻使用松花蛋时的涩味,可在食用时添加的调味品是食醋.
 )表示的粒子Cl;
)表示的粒子Cl; 碳和碳的氧化物在生产和生活中有着广泛的应用.
碳和碳的氧化物在生产和生活中有着广泛的应用.