题目内容
17. 1875年,法国化学家布瓦博德朗公布类铝他发现的新元素镓(元素符号为Ga)的性质:镓是银白色金属,能与沸水剧烈反应生成氢气和氢氧化镓.不久,他收到门捷列夫的来信称:镓就是我预言的“类铝”,其密度应在5.9/cm3-6.0g/cm3之间.
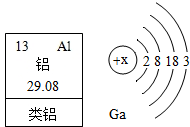
1875年,法国化学家布瓦博德朗公布类铝他发现的新元素镓(元素符号为Ga)的性质:镓是银白色金属,能与沸水剧烈反应生成氢气和氢氧化镓.不久,他收到门捷列夫的来信称:镓就是我预言的“类铝”,其密度应在5.9/cm3-6.0g/cm3之间.l876年,布瓦博德朗将金属镓提纯后测得镓的密度为5.94g/cm3,从而验证了元素周期表的正确性.随后科学家根据元素周期表的空位,按图索骥,发现了许多新元素.目前金属镓广泛用于制造半导体材料.镓的原子结构示意图如图,常见化合价为+3.
(1)镓元素的质子数为31;
(2)请根据上述材料,总结金属镓的物理性质:(答两点及以上给分)银白色、密度为5.94g/cm3、固体;
(3)氢氧化镓与氢氧化钠都具有碱的性质,则氢氧化镓与稀硫酸反应的化学式:3H2SO4+2Ga(OH)3=Ga2(SO4)3+6H2O.
分析 (1)根据在原子中,原子序数=核电荷数=质子数=核外电子数来分析;
(2)物理性质是指物质不需要发生化学变化就表现出来的性质;化学性质是指物质在化学变化中表现出来的性质;
(3)用知识迁移类推的方法,书写氢氧化镓与稀硫酸反应生成盐的化学式.因为镓元素原子最外层电子数为3,则其化合价为+3价;则氢氧化镓类比氢氧化铝,而氢氧化铝与硫酸反应的化学方程式为:3H2SO4+2Al(OH)3=Al2(SO4)3+6H2O.故可书写氢氧化镓与稀硫酸反应的化学方程式.
解答 解:(1)在原子中,核电荷数=质子数=核外电子数,X=2+8+18+3=31;故填:31;
(2)由题意可知,镓是银白色金属固体,密度4.7g/cm,不需要发生化学变化就表现出来的性质.属于物理性质;故填:银白色、密度为5.94g/cm3、固体;
(3)用知识迁移类推的方法,书写氢氧化镓与稀硫酸反应生成盐的化学式.因为镓元素原子最外层电子数为3,则其化合价为+3价;则氢氧化镓类比氢氧化铝,而氢氧化铝与硫酸反应化学方程式为:3H2SO4+2Al(OH)3=Al2(SO4)3+6H2O.故可书写氢氧化镓与稀硫酸反应的化学方程式3H2SO4+2Ga(OH)3=Ga2(SO4)3+6H2O.故填:3H2SO4+2Ga(OH)3=Ga2(SO4)3+6H2O.
点评 本题考查学生根据题中所给的信息及所学知识进行分析解题的能力,注意书写化学方程式的写配标等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
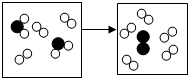
18.下列微观示意图中 和
和 分别表示氢原子和氧原子,下列说法正确的是( )
分别表示氢原子和氧原子,下列说法正确的是( )
 和
和 分别表示氢原子和氧原子,下列说法正确的是( )
分别表示氢原子和氧原子,下列说法正确的是( )
| A. | 参加反应的是两种物质 | B. | 反应物和生成物中只有一种单质 | ||
| C. | 化学变化中原子可分 | D. | 化学变化前后原子种类不变 |
8.同学们利用“硫酸、硝酸铵、氢氧化钠、碳酸钾”四种物质的溶液进行探究学习.请你们一起完成下列问题:
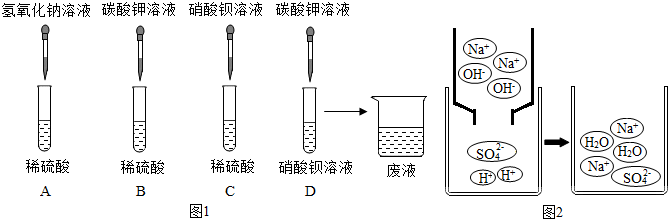
【实验探究】如图1,A、B、C、D四组同学分别进行了下列实验
(1)写出A中反应的化学方程式2NaOH+H2SO4=Na2SO4+2H2O:
【挖掘实质】如图2是A组反应的微观过程示意图.
(2)该反应的实质可以用化学符号表示为H++OH-=H2O;
【实践运用】完成试验后,四组同学将废液倒入同一个烧杯中,再将废液过滤,得到无色溶液和白色沉淀,用无色溶液滴加紫色石蕊试剂,变为红色.
(3)溶液中的白色沉淀一定是硫酸钡,理由是无色溶液滴加紫色石蕊试剂,变为红色,说明得到无色溶液为酸性,酸过量,亦说明白色沉淀不能溶于酸.
(4)从反应的试剂可以分析,废液中一定不含有的离子是OH-和CO32-.
(5)为了验证该溶液中可能含有的离子是否存在,我设计如下实验进行验证:

【实验探究】如图1,A、B、C、D四组同学分别进行了下列实验
(1)写出A中反应的化学方程式2NaOH+H2SO4=Na2SO4+2H2O:
【挖掘实质】如图2是A组反应的微观过程示意图.
(2)该反应的实质可以用化学符号表示为H++OH-=H2O;
【实践运用】完成试验后,四组同学将废液倒入同一个烧杯中,再将废液过滤,得到无色溶液和白色沉淀,用无色溶液滴加紫色石蕊试剂,变为红色.
(3)溶液中的白色沉淀一定是硫酸钡,理由是无色溶液滴加紫色石蕊试剂,变为红色,说明得到无色溶液为酸性,酸过量,亦说明白色沉淀不能溶于酸.
(4)从反应的试剂可以分析,废液中一定不含有的离子是OH-和CO32-.
(5)为了验证该溶液中可能含有的离子是否存在,我设计如下实验进行验证:
| 溶液中可能含有离子 | 实验步骤 | 实验现象 | 实验结论 |
| ①可能含有有Ba2+ | ②取滤液滴加硫酸钠溶液 | 现象明显 | 含有该离子 |
2.下列有关化学之最错误的是( )
| A. | 地壳中含量最多的非金属元素是氧元素 | |
| B. | 导电性最强的金属是金 | |
| C. | 金属活动顺序表中活动性最强的金属是钾 | |
| D. | 空气中含量最多的物质是氮气 |
9.粮食和人类生存发展密切相关.请根据所学的知识,回答下列问题:
(1)农作物生长过程张,需求量较大的营养元素是氮(填一种元素名称).
(2)农作物适合在中性或接近中性的土壤中生长,如果土壤呈酸性可加入适量的熟石灰来中和其酸性.
(3)请写出鉴别NH4Cl和K2SO4这两种化学肥料的实验方法、现象及实验结论:
(4)请你说出化肥过度施用产生的不良影响:会造成水体污染土壤污染和土壤板结.
(1)农作物生长过程张,需求量较大的营养元素是氮(填一种元素名称).
(2)农作物适合在中性或接近中性的土壤中生长,如果土壤呈酸性可加入适量的熟石灰来中和其酸性.
(3)请写出鉴别NH4Cl和K2SO4这两种化学肥料的实验方法、现象及实验结论:
| 实 验 方 法 | 实 验 现 象 和 结 论 |
6.水是生命活动不可缺少的物质.下列有关水的说法不正确的是( )
| A. | 长期饮用蒸馏水对健康有益 | |
| B. | 肥皂水可以区分软水和硬水 | |
| C. | 利用太阳能使水分解是最理想的氢能源 | |
| D. | 生活中通过煮沸可降低水的硬度 |
7.下列实验操作正确的是( )
| A. | 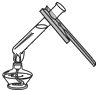 加热液体 | B. | 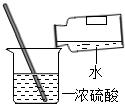 稀释浓硫酸 | C. | 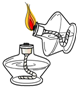 点燃酒精灯 | D. |  闻气体气味 |