题目内容
20.大豆是大众喜爱的食材之一,由大豆制作豆腐是中国古代一项重要发明,现成为全球颇 受欢迎的食品,豆腐中含有人们生活所需的各类营养素,每 100 克豆腐中含各种营养成分如表:| 成分 | 水 | 蛋白质 | 油脂 | X | 钙 | 铁 | 磷 | 维生素 B1 | 维生素 B2 |
| 质量(g) | 89.3 | 4.7 | 1.3 | 2.8 | 0.24 | 1.4 | 0.064 | 0.00006 | 0.00003 |
②豆腐中含有人体所需的微量元素是Fe
③豆腐制作的工艺流程中有一过程“点豆腐”,即在豆浆中加入某种盐,使溶解在水中蛋白质 溶解度变小而析出,据你分析,加入的盐可能是C.(填序号)
A.BaCl2B. CuSO4C. CaSO44D.AgNO3
④豆腐的制作时有一“煮浆”的过程,“煮浆”时用煤作燃料,通常将煤块加工成蜂窝煤,其 原因是增大接触面积,使充分燃烧,“煮浆”结束后,若不继续加煤,火焰会逐渐熄灭,原因是缺少可燃物
⑤大豆在生长过程需要施用复合肥,则你建议施用的化肥是C.(填序号)
A.KClB.(NH4)2SO4C.KH2PO4D.NH4NO3
⑥用大豆榨油时,油坊师傅身上衣服上油渍用清水很难洗去,但加入洗涤剂就很容易洗净,原因是洗涤剂具有乳化作用.
分析 ①根据人体必需的六大营养素来分析;②根据人体需要的微量元素来分析;③加入的盐必须是不会危害人体健康的;④根据促进燃烧的方法以及灭火的原理来分析;⑤根据化肥的分类来分析;⑥根据乳化原理来分析.
解答 解:①X的含量为2.8%,属于人体需要的营养素--糖类;故填:糖类;
②人体需要的微量元素有铁、碘、锌、硒等,故填:Fe;
③氯化钡、硫酸铜和硝酸银都是重金属盐,有毒,而硫酸钙没有毒,故填:C;
④将煤块加工成蜂窝煤,其原因是增大了煤炭与空气的接触面积,使煤炭能充分燃烧,“煮浆”结束后,若不继续加煤,火焰会逐渐熄灭,原因是缺少可燃物;故填:增大接触面积,使充分燃烧;缺少可燃物;
⑤氯化钾含有钾元素,属于钾肥;硫酸铵含有氮元素,属于氮肥;KH2PO4中含有磷元素和钾元素,属于复合肥;硝酸铵含有氮元素,属于氮肥;故填:C;
⑥用大豆榨油时,油坊师傅身上衣服上油渍用清水很难洗去,但加入洗涤剂就很容易洗净,原因是洗涤剂具有乳化作用.故填:乳化.
点评 解答本题要分析食物中的主要成分,然后再根据营养物质的分类进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
10.从图中获得的信息中错误的是( )


| A. | 空气是一种混合物 | B. | 氮气沸点比氧气高 | ||
| C. | 该过程属于物理变化 | D. | 氧气由氧分子构成 |
8.下列关于实验现象的描述,正确的是( )
| A. | 硫在空气中燃烧,产生明亮的蓝紫色火焰,生成一种有刺激性气味的气体 | |
| B. | 红磷在空气中燃烧时产生大量白色烟雾 | |
| C. | 加热氧化铜与木炭的混合物,红色粉末变黑,产生使澄清石灰水变浑浊的气体 | |
| D. | 向试管中的镁条滴加稀盐酸后,迅速产生大量气泡,同时试管壁发热 |
15.下列各组中的物质充分混合后,所得溶液的质量比反应前溶液的总质量减少的是( )
| A. | 锌和稀盐酸 | B. | 氢氧化铜和稀硫酸 | ||
| C. | 氢氧化钠溶液和硫酸铜溶液 | D. | 氯化钠溶液和稀盐酸 |
5.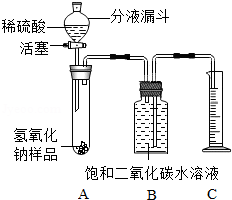 某化学课外小组的同学,为了测定实验室中一瓶因保存不善而部分变质的氢氧化钠中碳酸钠的质量分数,设计了如图所示的装置(图中铁架台已经略去),实验在27℃,101kPa下进行.
某化学课外小组的同学,为了测定实验室中一瓶因保存不善而部分变质的氢氧化钠中碳酸钠的质量分数,设计了如图所示的装置(图中铁架台已经略去),实验在27℃,101kPa下进行.
实验步骤如下:
①按图连接好装置;
②用天平准确称取氢氧化钠样品m g,放入A中试管内,向B中集气瓶内倒入饱和二氧化碳水溶液至瓶颈处;
③向分液漏斗中倒入稀硫酸,打开活塞,让稀硫酸滴入试管中至过量,关闭活塞.反应结束后,量筒中收集到饱和二氧化碳水溶液v mL.
④计算氢氧化钠样品中碳酸钠的质量分数.
请回答下列问题:
(1)准确判断氢氧化钠发生变质的实验现象是A中有气泡产生;写出氢氧化钠发生变质的化学方程式2NaOH+CO2═Na2CO3+H2O.
(2)在实验步骤①和②之间,还缺少一实验步骤,该实验步骤是:检查装置气密性.
(3)B中集气瓶盛装的饱和二氧化碳水溶液不能用水代替,其原因是:避免二氧化碳溶解在水里而损耗,造成测定结果偏低.
(4)判断实验步骤③中滴入的稀硫酸已过量的标志是滴入稀硫酸,A中不再有气泡产生.
(5)叙述检验氢氧化钠部分变质的方法:
(6)用上述装置不能准确测定已部分变质的氢氧化钠样品中氢氧化钠的质量分数,理由是氢氧化钠样品中除了碳酸钠,还有水.
(7)取10g变质的氢氧化钠于烧杯中,其中碳元素的质量分数为6%,向烧杯中加入100g一定质量分数的稀盐酸(足量),则反应结束后烧杯内物质的总质量是107.8g.
 某化学课外小组的同学,为了测定实验室中一瓶因保存不善而部分变质的氢氧化钠中碳酸钠的质量分数,设计了如图所示的装置(图中铁架台已经略去),实验在27℃,101kPa下进行.
某化学课外小组的同学,为了测定实验室中一瓶因保存不善而部分变质的氢氧化钠中碳酸钠的质量分数,设计了如图所示的装置(图中铁架台已经略去),实验在27℃,101kPa下进行.实验步骤如下:
①按图连接好装置;
②用天平准确称取氢氧化钠样品m g,放入A中试管内,向B中集气瓶内倒入饱和二氧化碳水溶液至瓶颈处;
③向分液漏斗中倒入稀硫酸,打开活塞,让稀硫酸滴入试管中至过量,关闭活塞.反应结束后,量筒中收集到饱和二氧化碳水溶液v mL.
④计算氢氧化钠样品中碳酸钠的质量分数.
请回答下列问题:
(1)准确判断氢氧化钠发生变质的实验现象是A中有气泡产生;写出氢氧化钠发生变质的化学方程式2NaOH+CO2═Na2CO3+H2O.
(2)在实验步骤①和②之间,还缺少一实验步骤,该实验步骤是:检查装置气密性.
(3)B中集气瓶盛装的饱和二氧化碳水溶液不能用水代替,其原因是:避免二氧化碳溶解在水里而损耗,造成测定结果偏低.
(4)判断实验步骤③中滴入的稀硫酸已过量的标志是滴入稀硫酸,A中不再有气泡产生.
(5)叙述检验氢氧化钠部分变质的方法:
| 实验步骤 | 实验现象 | 实验结论 |
| 1取样,溶于水,滴加过量的氯化钙溶液 | 产生白色沉淀 | 氢氧化钠部分变质 |
| 2静置,向上层清液中滴加酚酞溶液 | 变红色 |
(7)取10g变质的氢氧化钠于烧杯中,其中碳元素的质量分数为6%,向烧杯中加入100g一定质量分数的稀盐酸(足量),则反应结束后烧杯内物质的总质量是107.8g.
12.对于化学反应“甲+乙=丙+丁”,下列说法中错误的是( )
| A. | 若生成物丙和丁分别是盐和水,则反应物一定是酸和碱 | |
| B. | 若甲和丙是单质,乙和丁是化合物,则该反应一定属于置换反应 | |
| C. | 若甲、乙、丙均是化合物,则该反应不一定属于复分解反应 | |
| D. | 若甲、乙各取10g混合,使其充分反应,则丙、丁质量的总和不一定等于20g |
19.化学概念在逻辑上存在如图所示关系,下列概念间的关系说法正确是( )
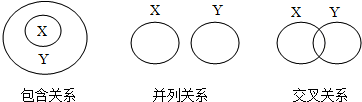

| A. | 纯净物与混合物属于包含关系 | |
| B. | 化合物与氧化物属于包含关系 | |
| C. | 单质与化合物属于交叉关系 | |
| D. | 金属元素和非金属元素属于并列关系 |
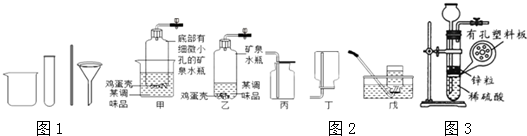
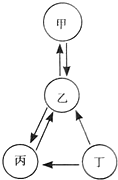 某同学构建了如图所示的转化关系图,其中甲、乙、丙、丁四种物质均含有碳元素,乙和丙的组成元素相同,乙中碳元素的质量分数约为27.27%.请回答下列问题:
某同学构建了如图所示的转化关系图,其中甲、乙、丙、丁四种物质均含有碳元素,乙和丙的组成元素相同,乙中碳元素的质量分数约为27.27%.请回答下列问题: