题目内容
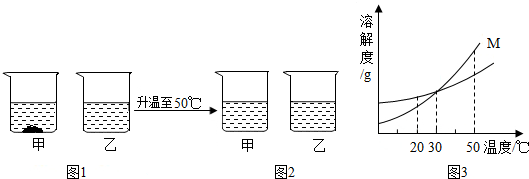
20℃时,将等质量不含结晶水的甲、乙固体分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2(不考虑水分蒸发),甲、乙固体的溶解度曲线如图3.下列说法错误的是( )

| A、图1中,甲一定是饱和溶液 |
| B、图2中,两溶液中溶质的质量分数一定相等 |
| C、图3中,M表示甲的溶解度曲线 |
| D、图2中,两溶液降温到30℃一定不会析出晶体 |
考点:饱和溶液和不饱和溶液,固体溶解度曲线及其作用,晶体和结晶的概念与现象
专题:溶液、浊液与溶解度
分析:A、根据饱和溶液的判断方法进行分析;
B、根据图2中均无固体剩余,说明全部溶解,相同质量的溶剂溶解了相同质量的溶质,并结合溶质的质量分数的计算公式进行分析;
C、根据图1中20℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,甲有固体剩余,说明甲的溶解度小于乙,结合图3中20℃时的溶解度进行分析;
D、根据图3可知两种物质的溶解度都随温度升高而增大,因此30℃时,甲、乙的溶解度都比20℃时大,且30℃时两物质的溶解度相等,再根据图1中信息可以知道20℃时乙中没有晶体析出进行分析.
B、根据图2中均无固体剩余,说明全部溶解,相同质量的溶剂溶解了相同质量的溶质,并结合溶质的质量分数的计算公式进行分析;
C、根据图1中20℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,甲有固体剩余,说明甲的溶解度小于乙,结合图3中20℃时的溶解度进行分析;
D、根据图3可知两种物质的溶解度都随温度升高而增大,因此30℃时,甲、乙的溶解度都比20℃时大,且30℃时两物质的溶解度相等,再根据图1中信息可以知道20℃时乙中没有晶体析出进行分析.
解答:解:A、图1中甲溶液中有固体剩余,所以甲是饱和溶液,故A正确;
B、图2中均无固体剩余,说明全部溶解,相同质量的溶剂溶解了相同质量的溶质,依据溶质质量分数=
×100%,所以图2中,两溶液中溶质的质量分数一定相等,故B正确;
C、图1中20℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,甲有固体剩余,说明在20℃时,甲的溶解度小于乙,从图3中的溶解度曲线可以看出,M表示甲的溶解度曲线,故C正确;
D、依据图3可知,两种物质的溶解度都随温度升高而增大,因此30℃时,甲、乙的溶解度都比20℃时大,且30℃时两物质的溶解度相等,依据图1中信息可以知道20℃时乙中没有晶体,在30℃时,乙中也不会有晶体析出,但是不能判断甲中是否有晶体析出,故D错误.
故选:D.
B、图2中均无固体剩余,说明全部溶解,相同质量的溶剂溶解了相同质量的溶质,依据溶质质量分数=
| 溶质质量 |
| 溶质质量+溶剂质量 |
C、图1中20℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,甲有固体剩余,说明在20℃时,甲的溶解度小于乙,从图3中的溶解度曲线可以看出,M表示甲的溶解度曲线,故C正确;
D、依据图3可知,两种物质的溶解度都随温度升高而增大,因此30℃时,甲、乙的溶解度都比20℃时大,且30℃时两物质的溶解度相等,依据图1中信息可以知道20℃时乙中没有晶体,在30℃时,乙中也不会有晶体析出,但是不能判断甲中是否有晶体析出,故D错误.
故选:D.
点评:本题难度不是很大,主要考查了固体溶解度曲线的意义及根据固体的溶解度曲线解决相关的问题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列实验操作正确的是( )
A、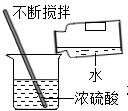 稀释浓硫酸 |
B、 加热固体 |
C、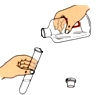 取用液体 |
D、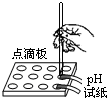 测定溶液pH |
分类是学习和研究化学物质及其变化的一种常用的基本方法.下列对物质分类正确的是( )
| A、水银和水都属于单质 |
| B、氯化钠和碳酸氢钠都属于盐 |
| C、硫酸和五氧化二磷都属于氧化物 |
| D、生石灰和熟石灰都属于碱 |
消防队员在草场灭火时,常使用风力灭火机,风力灭火机能灭火的原因是( )
| A、降低了草的着火点 |
| B、消除了可燃物 |
| C、隔绝了空气 |
| D、使燃着的草的温度降低 |
某小组同学打开瓶盖后没有闻到特殊气味.可推测该液体不可能是( )
| A、食盐水 | B、白醋 |
| C、纯净水 | D、澄清石灰水 |
如图为某反应的微观示意图,不同的球代表不同元素的原子,下列说法正确的是( )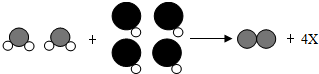

| A、该反应属于置换反应 |
| B、1个X分子中有3个原子 |
| C、反应物分子的个数比为1:1 |
| D、反应前后元素的化合价不改变 |
