题目内容
3.如表是元素周期表的部分内容,请认真分析并回答下面的问题:| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
| 3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(2)第6号元素与地壳中含量最多的元素可组成的一种物质是一氧化碳(或二氧化碳)(写名称),该物质中6号元素的化合价为+2(或+4)价.
(3)第3周期里有两种元素可构成我们生活中一种常见的调味品,其化学式是NaCl,构成该物质的微粒是c(填标号).
a.原子 b.分子 c.离子 d.电子
(4)第3周期中有一种元素的单质在空气中燃烧能发出耀眼白光,请写出该反应的化学方程式:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
(5)查得资料:在元素周期表中,同一纵行(族)的元素具有相似的化学性质.则下列各组元素具有相似化学性质的是a、d(填标号).
a.Li和Na b.C和N c.B和Mg d.Ne和Ar.
分析 (1)根据元素周期表的信息来分析;
(2)根据化合物的组成以及化合价的计算方法来分析;
(3)根据物质的组成以及结构来分析;
(4)根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写;
(5)根据同一纵行化学性质相似分析.
解答 解:(1)由元素周期表的信息可知,锂原子的核电荷数(原子序数)为3,相对原子质量为6.941;故填:3;相对原子质量;
(2)6号元素是碳元素,地壳中含量最高的元素为氧,二者可组成的化合物有一氧化碳和二氧化碳,其中碳元素的化合价分别为+2价、+4价;故填:一氧化碳(或二氧化碳);+2(或+4);
(3)第3周期里的钠元素与氯元素组成的氯化钠是一种常用调味品,氯化钠是由离子构成的;故填:NaCl;c;
(4)12号元素镁组成的单质是金属镁,镁带在空气中燃烧成氧化镁,反应的化学方程式为:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;故填:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;
(5)在元素周期表中,同一纵行(族)的元素具有相似的化学性质.
a、Li和Na 同在第一纵行,化学性质相似 b、C和N在同一横行,化学性质不相似c、B和Mg不在同一纵行,化学性质不相似 d、Ne和Ar在同一纵行,化学性质相似.
故选 a、d.
点评 本题考查学生根据元素周期表中所给信息应用到实际中解题的能力和有关化学用语的书写,难度较小.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.密闭容器内有X、O2、CO2、H2O四种物质,在一定条件下充分反应,测得反应前后各物质的质量如表.
下列说法中正确的是( )
| 物质 | X | O2 | CO2 | H2O |
| 反应前的质量/g | 23 | 60 | 44 | 0 |
| 反应后的质量/g | 待测 | 12 | 88 | 27 |
| A. | 反应后X的质量为0g | |
| B. | 该反应生成的二氧化碳和水的质量比为88:27 | |
| C. | 物质X的化学式一定为C2H6O | |
| D. | 该反应属于置换反应 |
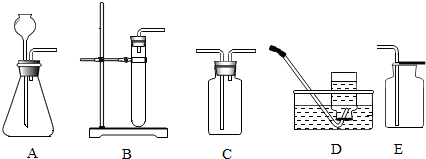
11.下图所示的实验基本操作正确的是( )
| A. |  放入固体颗粒 | B. |  熄灭酒精灯 | C. |  量取液体 | D. |  移走蒸发皿 |
18.以下有关溶液知识说法正确的是( )
| A. | 均一稳定的液体就是溶液 | B. | 汽油除油污是乳化作用 | ||
| C. | 雪地撒盐是为了提高凝固点 | D. | 浓溶液加水稀释后溶质质量不变 |
8.分类法是我们研究物质的基本方法.下列物质中,属于纯净物的是( )
| A. | 空气 | B. | 氮气 | C. | 澄清石灰水 | D. | 啤酒 |
13.除去下列各组物质中的杂质,所用试剂和方法均正确的是( )
| 物质 | 杂质 | 除杂质所用试剂和方法 | |
| A | H2 | HCl 气体 | 先通过足量 Na2CO3溶液,再通过浓硫酸 |
| B | KNO3溶液 | AgNO3溶液 | 先加入过量 KCl 溶液,再过滤 |
| C | KCl 固体 | K2CO3固体 | 加入少量 MnO2加热 |
| D | FeSO4溶液 | CuSO4溶液 | 先加过量 Fe 粉,再过滤 |
| A. | A | B. | B | C. | C | D. | D |
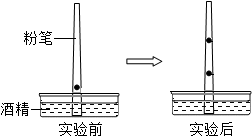 王刚在距一只粉笔的粗端2cm处点上一滴蓝墨水,将粉笔插入盛有酒精溶液的培养皿中.过了一段时间,他发现随着酒精的上升,蓝墨水也在粉笔上不断移动,最后蓝墨水在粉笔上分为两个区域,上半部分是蓝色,下半部分是紫色(如图所示).根据上述现象回答下列问题:
王刚在距一只粉笔的粗端2cm处点上一滴蓝墨水,将粉笔插入盛有酒精溶液的培养皿中.过了一段时间,他发现随着酒精的上升,蓝墨水也在粉笔上不断移动,最后蓝墨水在粉笔上分为两个区域,上半部分是蓝色,下半部分是紫色(如图所示).根据上述现象回答下列问题: