题目内容
12.t℃时,将10gA物质溶解在40g水中,30g溶液中含溶质B10g,C溶液的质量分数为30%,A、B、C三种溶液均恰好为饱和溶液,则三种物质在t℃时的溶解度大小顺序为( )| A. | .B>C>A | B. | .B>A>C | C. | .C>B>A |
分析 根据溶解度是指在一定温度下,在100g溶剂(一般是指水)中达到饱和状态时所溶解的溶质的质量解答.
解答 解:t℃时,将10gA物质溶解在40g水中,形成饱和溶液,即在t℃时,100g水中溶解25gA物质达到饱和,所以t℃时A物质的溶解度为25g;
t℃时,将30g溶液中含溶质B10g,形成饱和溶液,即在t℃时,100g水中溶解50gB物质达到饱和,所以t℃时B物质的溶解度为50g;
t℃时,C溶液的质量分数为30%,形成饱和溶液,即在t℃时,100g水中溶解42.9gC物质达到饱和,所以t℃时C物质的溶解度为42.9g;
所以则三种物质在t℃时的溶解度大小顺序为B>C>A.
故选:A.
点评 本题难度不大,主要考查了固体溶解度所表示的意义,通过本题可以加强学生对固体溶解度的理解,培养学生应用知识解决问题的能力.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
2.在下列变化中,属于氧化反应但不属于化合反应的是( )
| A. | 碳+氧气$\stackrel{点燃}{→}$二氧化碳 | B. | 酒精+氧气$\stackrel{点燃}{→}$二氧化碳+水 | ||
| C. | 氧化汞$\stackrel{加热}{→}$汞+氧气 | D. | 镁+氧气$\stackrel{点燃}{→}$氧化镁 |
20.在化学反应2A+B=2C中,设有6克A和B完全反应生成14克的C,若B的相对分子质量是32,则c 的相对分子质量为( )
| A. | 56 | B. | 28 | C. | 20 | D. | 44 |
7.如图为某反应的微观示意图,其中不同的球代表不同种类的原子.下列说法正确的是( )
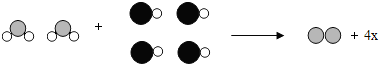

| A. | 反应前后元素种类发生了改变 | |
| B. | 1个X分子中有三个原子 | |
| C. | 两种反应物之间的质量比为1:2 | |
| D. | 各元素的化合价在反应前后均未改变 |
1.下列关于物质的组成和构成的说法中正确的是( )
| A. | 物质都是由多种元素组成 | B. | 含有不同元素的物质一定是化合物 | ||
| C. | 任何物质都是由一种元素组成 | D. | 物质并不都是由分子构成的 |
 某兴趣小组的同学用右图所示的装置测定空气中氧气的含量,先在瓶中装入少量某液体X,并将液面以上的空间分为5等份,实验结束,他们观察到瓶内液面到达图中“1”刻度处,且量筒中的水减少了44.8ml.
某兴趣小组的同学用右图所示的装置测定空气中氧气的含量,先在瓶中装入少量某液体X,并将液面以上的空间分为5等份,实验结束,他们观察到瓶内液面到达图中“1”刻度处,且量筒中的水减少了44.8ml.
