题目内容
20.如图为初中化学常见实验.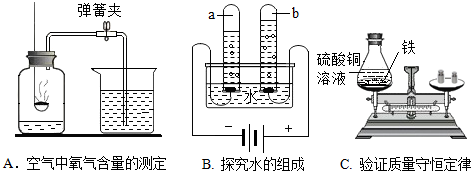
(1)实验A中,由进入集气瓶中的水的体积确定可燃物燃烧消耗氧气的体积.
(2)实验B中,a和b内的气体依次为H2、O2,该实验证明水是由氢、氧元素组成的.
(3)某小组进行实验C时,未在锥形瓶上塞橡胶塞,也验证了质量守恒定律,原因是空气中的物质不参加反应,且反应后没有物质逸出锥形瓶.
分析 (1)根据测定空气中氧气体积分数实验的原理及分析回答;
(2)根据电解水时,与正极相连的试管生成的气体是氧气,较少.与负极相连的试管生成的是氢气,较多,氢气的体积是氧气体积的2倍;
(3)根据空气中的物质不参加反应,且反应后没有物质逸出锥形瓶解答.
解答 解:(1)红磷燃烧消耗氧气,瓶内气压减小,烧杯中的水到吸入集气瓶中,由进入集气瓶中的水的体积确定可燃物燃烧消耗氧气的体积.
(2)电解水时,与正极相连的试管b生成的气体较少是氧气,与负极相连的试管a生成的气体较多是氢气,通过此实验证明水是由氢、氧两种元素组成的.
(3)铁和硫酸铜反应,生成铜和硫酸亚铁,空气中的物质不参加反应,且反应后没有物质逸出锥形瓶,故未在锥形瓶上塞橡胶塞,也验证了质量守恒定律.
答案:
(1)进入集气瓶中的水;
(2)H2、O2;氢、氧元素(H和O);
(3)空气中的物质不参加反应,且反应后没有物质逸出锥形瓶.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
相关题目
11.我国农村许多村庄道路两侧安装了太阳能路灯,关于太阳能路灯所用材料的叙述不正确的是( )

| A. | 铝合金灯柱属于金属材料 | |
| B. | 灯泡中填充氮气做保护气 | |
| C. | 透明的塑料灯罩属于有机合成高分子材料 | |
| D. | 硅电池板中的硅元素是地壳中含量最多的金属元素 |
5.钙是人体内含量最高的金属元素,未成年人需要摄入足够的钙促进骨骼的生长.下列食物中钙含量最低的是( )
| A. | 牛奶 | B. | 青菜 | C. | 豆类 | D. | 虾皮 |
12. 回答下列问题.
回答下列问题.
(1)如图是“504双吸剂”标签说明书(部分)
①食品包装袋中,被该双吸剂吸收的主要物质是O2、H2O(或氧气、水).
②部分失效的双吸剂中,有红棕色固体,其主要成分是Fe2O3(或氧化铁、三氧化二铁、铁锈).
③取少量双吸剂加入蒸馏水中,振荡后静置,测得上层清液的pH=9.双吸剂在水中发生反应的化学方程式:CaO+H2O═Ca(OH)2.
(2)如表是“某品牌碘盐”标签说明书(部分)
④说明书中碘酸钾(KIO3)属于人体所需六大营养素中的无机盐.
⑤工业上利用碘晶体(I2)与氯酸钾在一定条件下发生置换反应,可以制取碘酸钾.该反应的化学方程式:I2+2KClO3$\frac{\underline{\;一定条件\;}}{\;}$2KIO3+Cl2↑.
⑥推测碘酸钾的化学性质:受热易分解.
 回答下列问题.
回答下列问题.(1)如图是“504双吸剂”标签说明书(部分)
①食品包装袋中,被该双吸剂吸收的主要物质是O2、H2O(或氧气、水).
②部分失效的双吸剂中,有红棕色固体,其主要成分是Fe2O3(或氧化铁、三氧化二铁、铁锈).
③取少量双吸剂加入蒸馏水中,振荡后静置,测得上层清液的pH=9.双吸剂在水中发生反应的化学方程式:CaO+H2O═Ca(OH)2.
(2)如表是“某品牌碘盐”标签说明书(部分)
| 配料表 | 精制盐、碘酸钾、抗结剂 |
| 含碘量 | 40-60mg•kg-1 |
| 储存方法 | 密封、避光、防潮 |
| 食用方法 | 烹调时,待食品煮熟后加入 碘盐 |
⑤工业上利用碘晶体(I2)与氯酸钾在一定条件下发生置换反应,可以制取碘酸钾.该反应的化学方程式:I2+2KClO3$\frac{\underline{\;一定条件\;}}{\;}$2KIO3+Cl2↑.
⑥推测碘酸钾的化学性质:受热易分解.
10.下列变化中,属于化学变化的是( )
| A. | 海水晒盐 | B. | 瓷碗破碎 | C. | 食物腐败 | D. | 干冰升华 |

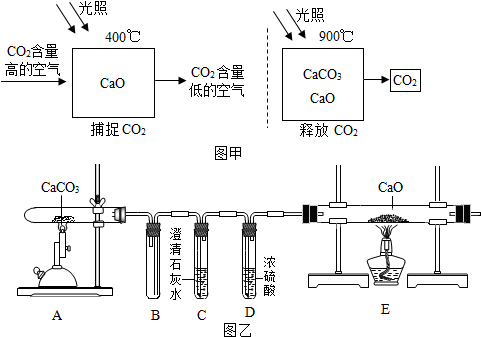
 金属在生活中应用广泛.
金属在生活中应用广泛.