题目内容
9.为了能及时发现煤气泄漏,常在煤气中加入少量有特殊气味的乙硫醇(C2H5SH).乙硫醇在煤气燃烧过程中可以充分燃烧,其化学方程式为2C2H5SH+9O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2X+6H2O 由此判断,下列说法正确的是( )| A. | 煤气是化合物 | |
| B. | 煤气燃烧不会污染空气 | |
| C. | X的相对分子质量为128 | |
| D. | 该反应中消耗的O2与生成的X的质量比为9:4 |
分析 根据题干提供的信息进行分析,煤气的主要成分是一氧化碳,属于混合物;根据质量守恒定律,化学反应前后原子的种类和个数不会改变即可判断X的化学式和计算反应中各物质的质量比.
解答 解:A、煤气的主要成分是一氧化碳,属于混合物,故A错误;
B、煤气的主要成分是一氧化碳,属于混合物,煤气燃烧会生成大量的二氧化碳以及固体颗粒,会污染空气故B错误;
C、由B分析可知,X是二氧化硫,其相对分子质量为64,故C错误;
D、反应中的O2与生成的X(二氧化硫)的质量比为9×32:64×2=9:4,故D正确.
故选:D.
点评 本题考查了常见物质的分类以及质量守恒定律的应用,完成此题,可以依据题干提供的信息结合已有的知识进行.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
19.下列反应既不是化合反应也不是分解反应的是( )
| A. | Fe+O2$\stackrel{点燃}{→}$Fe3O4 | B. | C+CO2$\stackrel{高温}{→}$2CO | ||
| C. | HgO$\stackrel{加热}{→}$Hg+O2 | D. | C2H2+O2$\stackrel{点燃}{→}$CO2+H2O |
 如图是“电解水实验”的装置图,根据所学知识回答问题:
如图是“电解水实验”的装置图,根据所学知识回答问题: 不同年龄段的群体每天钙的适宜摄入量不同,哺乳期妇女每日推荐摄入量为1200mg.如图为某保健品说明书的一部分,一片钙尔奇重3g,含碳酸钙50%请回答:
不同年龄段的群体每天钙的适宜摄入量不同,哺乳期妇女每日推荐摄入量为1200mg.如图为某保健品说明书的一部分,一片钙尔奇重3g,含碳酸钙50%请回答: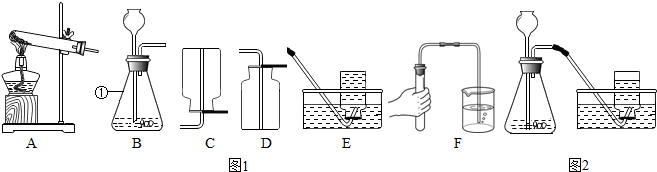
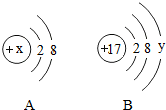 如图中A、B分别是某粒子的结构示意图,回答下列问题
如图中A、B分别是某粒子的结构示意图,回答下列问题