题目内容
3.空气、水是人类赖以生存的自然资源.(1)生活中常用肥皂水鉴别硬水和软水.
(2)热水瓶用久后,瓶胆内壁常附着一层水垢[主要成分是Mg(OH)2和CaCO3],可以用稀盐酸来洗涤,写出其与Mg(OH)2反应的化学方程式Mg(OH)2+2HCl=MgCl2+2H2O.
(3)水的电解实验中反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,此实验得出水是由氢元素和氧元素组成的结论.
(4)喝了汽水以后,经常会打嗝,这说明气体溶解度与温度有关.
分析 (1)根据鉴别硬水和软水的方法进行分析;
(2)根据酸的化学性质:能与碳酸盐反应生成盐、水和二氧化碳,与碱反应生成盐和水,写出反应的化学方程式即可;
(3)根据水通电分解生成氢气和氧气进行分析解答;
(4)根据气体的溶解度随温度的升高而减小,随着压强的增大而增大进行分析.
解答 解:(1)生活中可用肥皂水来区分硬水和软水,产生泡沫较多的是软水,产生泡沫较少、浮渣多的是硬水;
(2)热水瓶瓶胆内壁常附着一层水垢(主要成分是碳酸钙和氢氧化镁),能与盐酸反应,则水垢可以用试剂盐酸来洗涤;盐酸与氢氧化镁反应生成氯化镁和水,反应的方程式为:Mg(OH)2+2HCl=MgCl2+2H2O;
(3)水通电分解生成氢气和氧气,反应的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;根据以上实验事实可知:水是由氢、氧元素组成的;
(4)喝了汽水以后会打饱嗝,是由于胃内的温度高,二氧化碳的溶解度变小而导致的,说明了气体溶解度随着温度升高而降低.
故答案为:(1)肥皂水;(2)稀盐酸;Mg(OH)2+2HCl=MgCl2+2H2O;(3)2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;氢元素和氧元素;(4)温度.
点评 此题考查知识点较多,综合性较强,可依据已有的知识进行解答.

练习册系列答案
相关题目
13.“雨花茶”盛产于南京雨花台,叶绿圆润.绿茶中的单宁酸具有清热解毒、抗癌等功效,其化学式为C76H52O46,下列关于单宁酸的说法不正确的是( )
| A. | 单宁酸由碳、氢、氧三种元素组成 | |
| B. | 单宁酸不属于氧化物 | |
| C. | 单宁酸是由76个碳原子、52个氢原子和46个氧原子构成 | |
| D. | 单宁酸是由单宁酸分子构成 |
11.下列图象不能正确反映其对应关系的是( )
| A. | 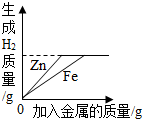 向等质量的锌粉和铁粉中加入过量的稀硫酸 | |
| B. | 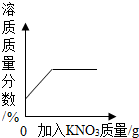 向一定量KNO3的不饱和溶液中不断加入KNO3固体 | |
| C. | 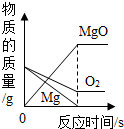 等质量的镁和氧气在点燃条件下充分反应 | |
| D. | 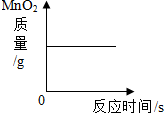 过氧化氢溶液与二氧化锰混合 |
18.下列叙述中正确的个数是( )
①化学变化不但生成其他物质,而且还伴随着能量的变化
②人类利用的能量都是通过化学反应获得的
③石油是一种化工产品
④可燃物在任何条件下燃烧都会发生爆炸
⑤化学反应过程中都会发生放热现象.
①化学变化不但生成其他物质,而且还伴随着能量的变化
②人类利用的能量都是通过化学反应获得的
③石油是一种化工产品
④可燃物在任何条件下燃烧都会发生爆炸
⑤化学反应过程中都会发生放热现象.
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
15.下列关于物质组成中“一定”的说法不正确的是( )
| A. | 合金中一定有金属元素 | B. | 氧化物中一定有氧元素 | ||
| C. | 酸、碱中一定有氢元素 | D. | 盐中一定有金属元素 |
12.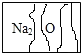 实验室有了瓶标签受到腐蚀(如图所示)的无色溶液,各学习小组开展探究.
实验室有了瓶标签受到腐蚀(如图所示)的无色溶液,各学习小组开展探究.
【提出问题】这瓶无色溶液究竟是什么物质的溶液?
【猜想与假设】经了解得知,这瓶无色溶液原是放在存放盐溶液的柜子里.由此猜测:可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中某一种的溶液.
【理论分析】为了确定该溶液,他们首先进行了分析:
(1)甲同学根据标签上的组成元素认为一定不可能是氯化钠溶液.
(2)乙同学提出,碳酸氢钠、硝酸钠的溶液也不可能,他的依据是碳酸氢钠和硝酸钠的化学式中钠元素右下角的数字为1.
【设计实验】为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如表实验.
【实验结论】
(3)该瓶无色溶液的溶质是碳酸钠.生成白色沉淀的化学方程式是Na2CO3+BaCl2=BaCO3↓+2NaCl.
【实验反思】
(4)丙同学认为原设计的实验还可简化,同样达到鉴别的目的.丙同学设计的实验如下(将实验操作及实验现象填入相应的空格中):
发生反应的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑.
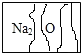 实验室有了瓶标签受到腐蚀(如图所示)的无色溶液,各学习小组开展探究.
实验室有了瓶标签受到腐蚀(如图所示)的无色溶液,各学习小组开展探究.【提出问题】这瓶无色溶液究竟是什么物质的溶液?
【猜想与假设】经了解得知,这瓶无色溶液原是放在存放盐溶液的柜子里.由此猜测:可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中某一种的溶液.
【理论分析】为了确定该溶液,他们首先进行了分析:
(1)甲同学根据标签上的组成元素认为一定不可能是氯化钠溶液.
(2)乙同学提出,碳酸氢钠、硝酸钠的溶液也不可能,他的依据是碳酸氢钠和硝酸钠的化学式中钠元素右下角的数字为1.
【设计实验】为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如表实验.
| 实验操作 | 实验现象 |
| ①取少量该无色溶液于试管中,慢慢滴加BaCl2溶液 ②静置后,再去上层清液,向沉淀中滴加稀盐酸 | 产生白色沉淀 产生大量气泡,沉淀消失 |
(3)该瓶无色溶液的溶质是碳酸钠.生成白色沉淀的化学方程式是Na2CO3+BaCl2=BaCO3↓+2NaCl.
【实验反思】
(4)丙同学认为原设计的实验还可简化,同样达到鉴别的目的.丙同学设计的实验如下(将实验操作及实验现象填入相应的空格中):
| 实验操作 | 实验现象 |
13.下列各组物质中,都是由分子构成的一组是( )
| A. | 金刚石和金 | B. | 氯化钠和氯化氢 | C. | 冰和干冰 | D. | 汞和硫酸铜 |