题目内容
7.化学兴趣小组在老师指导下对碳酸钠、碳酸氢钠进行了深入的探究.实验探究Ⅰ:碳酸钠、碳酸氢钠受热能否分解
【实验步骤】
(1)在两支试管里分别装入适量的碳酸钠、碳酸氢钠粉末,并在试管内壁粘贴干燥的蓝色石蕊试纸.
(2)按图1连好实验装置,并调节杠杆处于水平状态.
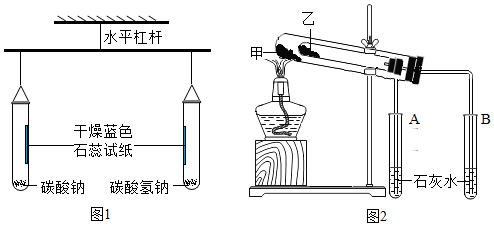
(3)点燃酒精灯,先加热左端试管里的碳酸钠2分钟,杠杆保持水平,干燥的蓝色石蕊试纸不变色.说明碳酸钠受热不分解(填“分解”或“不分解”).
(4)然后加热右端试管里的碳酸氢钠2分钟,发现干燥的蓝色石蕊试纸变成红色、杠杆的右端上升(填“上升”或“下降”),说明碳酸氢钠受热分解.
【拓展延伸】
(1)验证碳酸钠、碳酸氢钠的热稳定性,也可用图2所示的装置.在加热过程中,观察到A试管中无明显现象、B试管中石灰水变浑浊,说明乙物质是小苏打(填写俗称).
(2)结合以上实验现象及质量守恒定律,完成碳酸氢钠分解的化学方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
实验探究Ⅱ:碳酸氢钠受热后残留固体的成分
【提出猜想】
根据碳酸氢钠受热分解的化学方程式,不难作出如下3个猜想:
①仅有碳酸氢钠;②仅有碳酸钠;③碳酸钠和碳酸氢钠的混合物.
【实验验证】
(1)取碳酸氢钠受热后的残留固体1.68g,充分加热一段时间;冷却后再次称量固体质量,约为1.23g.
(2)通过推算可知,猜想③成立.
分析 碳酸氢钠俗称小苏打,受热分解生成碳酸钠、水和二氧化碳,碳酸钠受热不分解.
解答 解:【实验步骤】
(3)点燃酒精灯,先加热左端试管里的碳酸钠2分钟,杠杆保持水平,干燥的蓝色石蕊试纸不变色.说明碳酸钠受热不分解.
故填:不分解.
(4)然后加热右端试管里的碳酸氢钠2分钟,发现干燥的蓝色石蕊试纸变成红色,说明反应生成了水和二氧化碳,水和二氧化碳反应生成碳酸,碳酸干燥的蓝色石蕊试纸变成红色,因为反应生成了水蒸气和二氧化碳,从而使杠杆的右端上升,说明碳酸氢钠受热分解.
故填:上升.
【拓展延伸】
(1)在加热过程中,观察到A试管中无明显现象、B试管中石灰水变浑浊,说明乙物质是小苏打,小苏打受热分解生成了二氧化碳,从而使澄清石灰水变浑浊.
故填:小苏打.
(2)碳酸氢钠分解生成碳酸钠、水和二氧化碳,反应的化学方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
故填:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
【提出猜想】
根据碳酸氢钠受热分解的化学方程式,可以作出如下3个猜想:
①仅有碳酸氢钠;②仅有碳酸钠;③碳酸钠和碳酸氢钠的混合物.
故填:碳酸钠.
【实验验证】
取碳酸氢钠受热后的残留固体中一定含有碳酸钠,1.68g固体充分加热一段时间;冷却后再次称量固体质量约为1.23g,固体质量减小,说明原固体中含有碳酸氢钠,因此猜想③成立.
故填:③.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
2.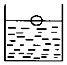 如图在室温下的饱和硝酸钾溶液中放了一个塑料小球.以下做法能使小球下沉的是( )
如图在室温下的饱和硝酸钾溶液中放了一个塑料小球.以下做法能使小球下沉的是( )
 如图在室温下的饱和硝酸钾溶液中放了一个塑料小球.以下做法能使小球下沉的是( )
如图在室温下的饱和硝酸钾溶液中放了一个塑料小球.以下做法能使小球下沉的是( )| A. | 加入少量硝酸钾晶体,充分搅拌 | B. | 蒸发一些溶剂,恢复到室温 | ||
| C. | 升高温度,使硝酸钾晶体析出 | D. | 降低温度,使硝酸钾晶体析出 |
12.某校化学课外活动小组在一次活动中,取刚降到地面的雨水水样,每隔5分钟用pH计测定一次pH,其数据如下表:
已知:正常雨水的pH约为5.6,酸雨的pH小于5.6
(1)所取的雨水是否为酸雨是(填“是”或“否”);在测定期间,雨水水样的酸性随着时间的变化逐渐增强(填“增强”或“减弱”)
(2)经调查,这一地区有一座燃煤发电厂(生产过程中产生SO2),某同学设计用火碱来吸收生产过程中产生的SO2,将其转化成亚硫酸钠(Na2SO3).请你帮他写出该反应的化学方程式:SO2+2NaOH═Na2SO3+H2O
(3)为了防止“酸雨”的产生,保护我们的大自然,请提出一条合理化的建议:硫酸厂产生的尾气处理后再排放,煤燃烧前先脱硫.
(4)若用pH试纸测定雨水的酸碱度,测定方法是:用玻璃棒沾取雨水样品滴在pH试纸上,将pH试纸所显示的颜色与标准比色卡对比,读出数值.
| 测定时刻 | 6:05 | 6:10 | 6:15 | 6:20 | 6:25 | 6:30 |
| pH | 4.95 | 4.94 | 4.94 | 4.88 | 4.86 | 4.85 |
(1)所取的雨水是否为酸雨是(填“是”或“否”);在测定期间,雨水水样的酸性随着时间的变化逐渐增强(填“增强”或“减弱”)
(2)经调查,这一地区有一座燃煤发电厂(生产过程中产生SO2),某同学设计用火碱来吸收生产过程中产生的SO2,将其转化成亚硫酸钠(Na2SO3).请你帮他写出该反应的化学方程式:SO2+2NaOH═Na2SO3+H2O
(3)为了防止“酸雨”的产生,保护我们的大自然,请提出一条合理化的建议:硫酸厂产生的尾气处理后再排放,煤燃烧前先脱硫.
(4)若用pH试纸测定雨水的酸碱度,测定方法是:用玻璃棒沾取雨水样品滴在pH试纸上,将pH试纸所显示的颜色与标准比色卡对比,读出数值.
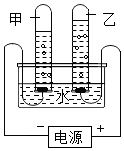 如图是电解水实验的实验装置
如图是电解水实验的实验装置
 用“●、○”分别表示两种不同的原子,如图是表示气体A可以在气体B中燃烧生成气体C的化学变化模型示意图,实验室制取气体C常用稀盐酸与石灰石反应
用“●、○”分别表示两种不同的原子,如图是表示气体A可以在气体B中燃烧生成气体C的化学变化模型示意图,实验室制取气体C常用稀盐酸与石灰石反应