题目内容
根据如图甲回答问题(1)~(3).
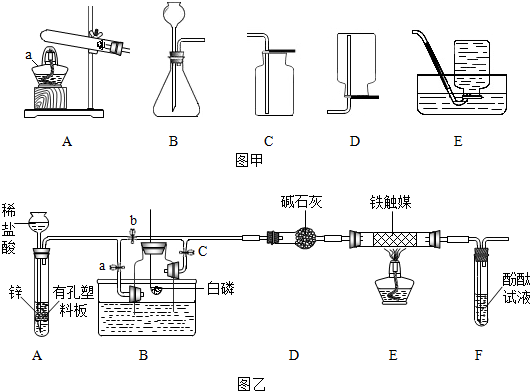
(1)实验仪器a的名称是 .
(2)实验室用高锰酸钾制取氧气的化学方程式为 ,所用的发生装置是 .用E收集氧气与C相比的优点是 (写出一点).
(3)实验室制取并收集二氧化碳选用的装置是 ,检验二氧化碳是否收集满的方法是 .
(4)化学小组的同学设计了如图乙所示的装置用于制取少量氨气.完成以下实验操作中的相关问题:
(1)检查装置气密性
(2)关闭a、c,打开b,从长颈漏斗加入稀盐酸,A中发生反应的化学方程式为 .在F的出口处收集氢气并验纯.
(3)关闭c,在盛满空气的多孔玻璃钟罩内用激光点燃足量的白磷.反应的化学方程式为 .
(4)待多孔玻璃钟罩冷却到室温,打开a,观察到的现象是 .
(5)点燃酒精灯加热玻璃管E,并打开C.氢气和氮气在铁触媒的催化作用下生成氨气,反应的化学方程式为 . 实验过程中D装置的作用是 .

(1)实验仪器a的名称是
(2)实验室用高锰酸钾制取氧气的化学方程式为
(3)实验室制取并收集二氧化碳选用的装置是
(4)化学小组的同学设计了如图乙所示的装置用于制取少量氨气.完成以下实验操作中的相关问题:
(1)检查装置气密性
(2)关闭a、c,打开b,从长颈漏斗加入稀盐酸,A中发生反应的化学方程式为
(3)关闭c,在盛满空气的多孔玻璃钟罩内用激光点燃足量的白磷.反应的化学方程式为
(4)待多孔玻璃钟罩冷却到室温,打开a,观察到的现象是
(5)点燃酒精灯加热玻璃管E,并打开C.氢气和氮气在铁触媒的催化作用下生成氨气,反应的化学方程式为
考点:常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,二氧化碳的实验室制法,二氧化碳的检验和验满,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:酒精灯是常用的加热仪器,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;锌和盐酸反应生成氯化锌和氢气,磷和氧气在点燃的条件下生成五氧化二磷,配平即可;待多孔玻璃钟罩冷却到室温,打开a,观察到的现象是:水面上升,约占液面以上钟罩容积的五分之一;氢气和氮气在铁触媒的催化作用下生成氨气,配平即可;实验过程中D装置的作用是:干燥作用.
解答:解:图甲中:(1)酒精灯是常用的加热仪器,故答案为:酒精灯;
(2)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净;故答案为:2KMnO4
K2MnO4+MnO2+O2↑;A;收集的氧气比较纯净;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;故答案为:BC;将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;
图乙中:(2)锌和盐酸反应生成氯化锌和氢气,配平即可,故答案为:Zn+2HCl=ZnCl2+H2↑;
(3)磷和氧气在点燃的条件下生成五氧化二磷,配平即可;故答案为:4P+5O2
2P2O5
(4)待多孔玻璃钟罩冷却到室温,打开a,观察到的现象是:水面上升,约占液面以上钟罩容积的五分之一,故答案为:水面上升,约占液面以上钟罩容积的五分之一;
(5)氢气和氮气在铁触媒的催化作用下生成氨气,配平即可;实验过程中D装置的作用是:干燥作用;故答案为:3H2+N2
2NH3;干燥作用;
(2)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净;故答案为:2KMnO4
| ||
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;故答案为:BC;将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;
图乙中:(2)锌和盐酸反应生成氯化锌和氢气,配平即可,故答案为:Zn+2HCl=ZnCl2+H2↑;
(3)磷和氧气在点燃的条件下生成五氧化二磷,配平即可;故答案为:4P+5O2
| ||
(4)待多孔玻璃钟罩冷却到室温,打开a,观察到的现象是:水面上升,约占液面以上钟罩容积的五分之一,故答案为:水面上升,约占液面以上钟罩容积的五分之一;
(5)氢气和氮气在铁触媒的催化作用下生成氨气,配平即可;实验过程中D装置的作用是:干燥作用;故答案为:3H2+N2
| ||
| △ |
点评:本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和气体的验满方法等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
小王同学用排水法收集了一瓶氧气,经检验氧气中混有氮气,你认为不可能的原因是( )
| A、导管刚冒出气泡就开始收集气体 |
| B、集气瓶未事先装满水留有气泡 |
| C、集气瓶收集满气体后拿出水槽,再盖好毛片玻璃 |
| D、集气瓶内水未排尽就盖好毛玻璃拿出水槽,正放在桌面上 |
小明同学在实验室过氧化氢溶液的方法制取氧气,他忘记加二氧化锰,结果是( )
| A、放出氧气总量减少 |
| B、无氧气放出 |
| C、有氧气放出,但速度慢 |
| D、有氧气放出,但速度慢且量少 |
一包不纯的Na2CO3固体,杂质可能是CaCl2、NaCl、NaHCO3中的一种或几种.现取该样品溶于水得到澄清溶液;另取样品10.6g,加入100g稀盐酸恰好完全反应,产生气体4g,则下列判断不正确的是( )
| A、加水得澄清溶液,样品中一定没有CaCl2 |
| B、样品中一定含有NaCl,可能含有NaHCO3 |
| C、样品中一定含有NaHCO3,可能含有NaCl |
| D、所加的稀盐酸溶质质量分数大于7.3% |
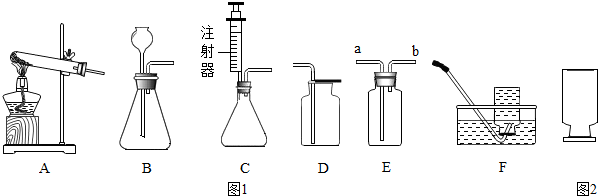
 如图是电解水的两个装置,回答下列问题:
如图是电解水的两个装置,回答下列问题: