题目内容
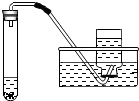
实验探究证明酒精灯燃烧后,只有水和二氧化碳生成,则酒精这种物质中所含的元素
[ ]
A.一定含有碳、氢、氧三种元素
B.一定含有碳、氢两种元素
C.只含碳、氢两种元素
D.无法确定
答案:B
解析:
提示:
解析:
|
思路与技巧:燃烧后生成水和二氧化碳,说明物质和氧发生了氧化反应.生成物水中的氢元素和生成物二氧化碳中的碳元素一定来源于原物质;但水和二氧化碳中的氧元素的来源则可能有两种情况:一是原物质中不含氧元素,例如甲烷CH4,它燃烧时生成的水和二氧化碳中的氧元素,全部来自于燃烧时消耗的氧气;第二种情况是,原物质中含有氧元素,如乙醇C2H5OH,它燃烧时生成的水和二氧化碳中的氧元素一部分是来源于燃烧过程中消耗的氧气,另一部分来自本身含有的氧元素.综上所述:燃烧后只生成水和二氧化碳的物质,其组成中一定含有碳元素和氢元素.而氧元素,可能含有,也可能不含有. |
提示:
|
评析:探究实验的结果只能说明酒精只含碳、氢两种元素,要想确定其组成中是否含氧元素,要通过计算来判断,若生成物中所含的氧元素等于消耗的氧气质量,则原物质中不含氧元素;若生成物中所含氧元素大于所消耗的氧气质量,则原物质中一定含氧元素. |

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目

 B、
B、 C、
C、
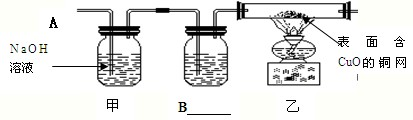
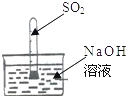 他的理由是
他的理由是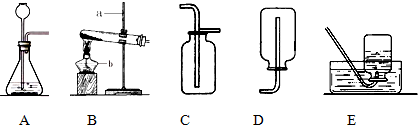
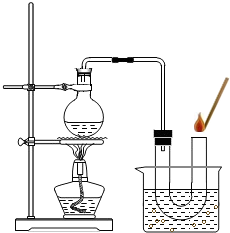 (1)碳酸钙的化学符号为
(1)碳酸钙的化学符号为