题目内容
7.如图所示图象能正确反映其对应关系的是( )| A. | 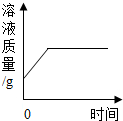 某温度下,向一定量饱和的氯化钠溶液中加入氯化钠固体 | |
| B. | 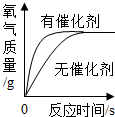 用一定量的过氧化氢溶液制取氧气 | |
| C. |  向等质量的锌粉和铁粉中分别滴加质量分数相同的足量稀盐酸 | |
| D. | 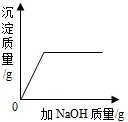 向硫酸和硫酸铜的混合液中滴加氢氧化钠溶液 |
分析 A、根据饱和溶液的定义来进行分析;
B、根据催化剂的定义进行分析;
C、根据向等质量的锌粉和铁粉中分别滴加质量分数相同的足量稀盐酸,金属是过量的,所以金属与酸反应速率相同,铁生成的氢气多进行分析;
D、根据硫酸铜和氢氧化钠反应过程分析.
解答 解:A、氯化钠溶液已饱和,所以再加入氯化钠固体,氯化钠不会溶解,所以溶质的质量也不会改变,故错误;
B、催化剂只会改变反应速率,不会影响生成物的量,故正确;
C、向等质量的锌粉和铁粉中分别滴加质量分数相同的足量稀盐酸,金属是过量的,所以金属与酸反应速率相同,铁生成的氢气多,应为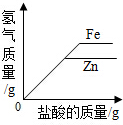 ;故错误;
;故错误;
D、由于中和反应优先发生,只有硫酸完全反应之后,氢氧化钠才能与硫酸铜反应生成氢氧化铜沉淀,应为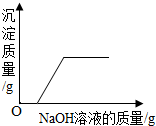 ,故错误;
,故错误;
故选:B.
点评 本题是过程与图象结合题,是对学生识图能力的考查,解题的关键是能正确的分析各个反应的过程,并结合图象分析问题,对培养学生分析问题的能力有一定帮助.

练习册系列答案
相关题目
15.配制一定溶质质量分数溶液的步骤是( )
| A. | 溶解、计算、称量 | B. | 溶解、过滤、计算 | C. | 计算、称量、溶解 | D. | 计算、溶解、称量 |
2.学习化学可以了解日常生活中某些变化的本质,下列变化中属于化学变化的是( )
| A. | 钢丝球刷锅 | B. | 西瓜榨成汁 | C. | 海水晒盐 | D. | 番薯酿成酒 |
12.研究和控制化学反应条件有重要意义.
(1)同学们想探究双氧水的溶质质量分数对反应速率的影响,在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
①取用二氧化锰的仪器是图1中的B(选填编号).
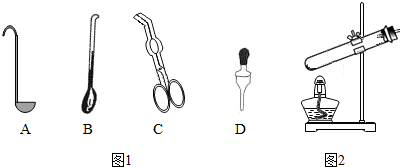
②写出上述反应的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
③实验3中,加入的二氧化锰质量为5g.
④相同条件下,实验3产生氧气的速率最快,说明相同条件下,反应物浓度越大,反应速率越快.
(2)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择图2装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,同学分析原因后,采用了排水法收集气体,再检验,证明加热双氧水也可产生氧气.
(1)同学们想探究双氧水的溶质质量分数对反应速率的影响,在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
| 实验 | 30%双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 | 5 | 67 |

②写出上述反应的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
③实验3中,加入的二氧化锰质量为5g.
④相同条件下,实验3产生氧气的速率最快,说明相同条件下,反应物浓度越大,反应速率越快.
(2)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择图2装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,同学分析原因后,采用了排水法收集气体,再检验,证明加热双氧水也可产生氧气.
19.燃烧是生活中一种常见的现象.下列有关燃烧的说法错误的是( )
| A. | 氢气可以在氯气中燃烧,说明燃烧不一定要有氧气参与 | |
| B. | 碳、磷在氧气中燃烧比在空气中燃烧剧烈 | |
| C. | 燃烧是可燃物与氧气发生的一种剧烈的发光、放热的氧化反应 | |
| D. | 在空气中不能燃烧的物质在氧气中也不能燃烧 |
16.以下不能与水混合产生溶液的是( )
| A. | 可乐 | B. | 稀盐酸 | C. | 食用油 | D. | 蔗糖 |
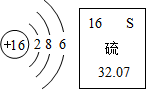 根据图示信息判断,下列说法正确的是C
根据图示信息判断,下列说法正确的是C