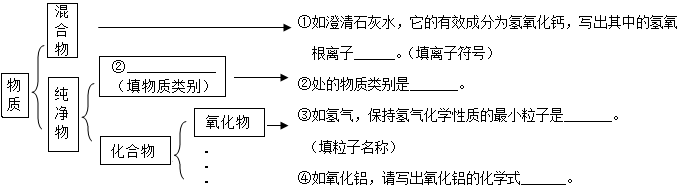
题目内容
17.某化学兴趣小组在实验室做了如图所示的A、B两个实验.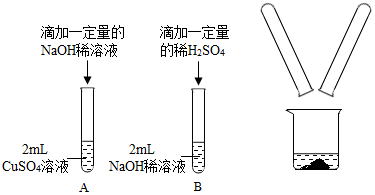
(1)B实验中发生反应的化学方程式为2NaOH+H2SO4=Na2SO4+2H2O.
(2)A、B两个实验结束后,小组同学将两支试管中的物质同时倒入一洁净的烧杯中(如图所示),混合后,观察到烧杯中有蓝色沉淀.同学们将烧杯内的物质过滤,对所得滤液中溶质的成分进行探究.
【猜想】小明猜想:滤液中的溶质是Na2SO4、CuSO4:
小光猜想:滤液中的溶质是Na2SO4、NaOH;
小英猜想:滤液中的溶质是Na2SO4、CuSO4、H2SO4;
你的猜想:滤液中的溶质还可能是Na2SO4.
【讨论】你认为小英的猜想一定不合理.如果滤液为无色,还可排除小明的猜想,理由是滤液中含有硫酸铜,溶液呈蓝色.
分析 根据已有的知识进行分析,氢氧化钠能与硫酸反应生成硫酸钠和水;硫酸铜能与氢氧化钠反应生成氢氧化铜沉淀,氢氧化铜能与硫酸反应生成硫酸铜和水;硫酸铜溶液呈蓝色,据此解答.
解答 解:(1)氢氧化钠能与硫酸反应生成硫酸钠和水,反应的方程式是:2NaOH+H2SO4=Na2SO4+2H2O;故填:2NaOH+H2SO4=Na2SO4+2H2O.
(2)【猜想】硫酸铜能与氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,氢氧化钠能与硫酸反应生成硫酸钠,故滤液中一定含有硫酸钠,当A中的氢氧化钠与硫酸铜恰好反应,B中的氢氧化钠与硫酸恰好反应,我的猜想是滤液中的溶质只有Na2SO4;故填:Na2SO4.
【讨论】由于烧杯中含有蓝色沉淀氢氧化铜,而氢氧化铜能与硫酸反应生成易溶于水的硫酸铜,故一定不会含有硫酸,所以小英的猜想一定不正确;硫酸铜溶液是蓝色的,若滤液是无色的,则小明的猜想不正确,故填:小英,小明,滤液中含有硫酸铜,溶液呈蓝色.
点评 本题考查了常见的物质的性质,完成此题,可以依据已有的知识进行.要求同学们加强对基础知识的储备,以便灵活应用.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
6.下列反应的文字表达式中,既不是化合反应,也不是分解反应的是( )
| A. | 碳+氧气$\stackrel{点燃}{→}$二氧化碳 | B. | 磷+氧气$\stackrel{点燃}{→}$五氧化二磷 | ||
| C. | 石蜡+氧气二$\stackrel{点燃}{→}$氧化碳+水 | D. | 过氧化氢$\stackrel{二氧化锰}{→}$水+氧气 |
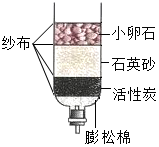 我国偏远地区水资源并不丰富,有些村民用地下水作为生活用水,人们常用肥皂水检验地下水是硬水还是软水;生活中可用煮沸的方法降低水的硬度;某同学自制如图所示简易净水器,图中小卵石、石英砂的主要作用是过滤,活性炭的主要起吸附作用.
我国偏远地区水资源并不丰富,有些村民用地下水作为生活用水,人们常用肥皂水检验地下水是硬水还是软水;生活中可用煮沸的方法降低水的硬度;某同学自制如图所示简易净水器,图中小卵石、石英砂的主要作用是过滤,活性炭的主要起吸附作用.