题目内容
11. 甲、乙、丙三种物质的溶解度曲线如图所示.据图回答:
甲、乙、丙三种物质的溶解度曲线如图所示.据图回答:(1)曲线甲和乙的交点所表示的含义为在40℃时,物质甲和乙的溶解度相等.
(2)要使接近饱和的丙物质溶液变为饱和,可采取的一种措施是增加溶质(或蒸发溶剂或升高温度).
(3)当甲的饱和溶液中混有少量的乙时,可采用冷却热饱和溶液方法提纯甲物质.
(4)在50℃时,用质量相同的甲、乙、丙三种物质分别配制饱和溶液,所得饱和溶液质量最大的是丙.
(5)将60℃的等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃时,析出晶体最多的是甲.
分析 (1)溶解度曲线相交于一点时,表示此时两物质的溶解度相等;
(2)根据丙的溶解度随温度的变化解答;
(3)由溶解度曲线图,对比甲、乙两物质溶解度受温度影响大小,判断将甲物质从甲和乙少量的混合物中分离出来宜采用的方法;
(4)根据物质的溶解度曲线、溶质质量、溶剂质量可以判断配制的溶液质量大小;
(5)根据物质的溶解度随温度的变化情况,可以比较将饱和溶液降低温度时析出晶体的多少.
解答 解:(1)根据溶解度曲线图,两物质的溶解度曲线在40℃交于点m,表示40℃甲与乙的溶解度相等;
(2)要使接近饱和的丙物质溶液变为饱和,可采取的一种措施是增加溶质(或蒸发溶剂或升高温度);
(3)根据两物质的溶解度曲线,物质甲溶解度受温度影响较大而物质乙的溶解度受温度影响不大,因此,将甲物质从甲和乙少量的混合物中分离出来,宜采用降温结晶(冷却热饱和溶液);
(4)在50℃时,甲乙丙的溶解度大小是甲>乙>丙,因此用质量相同的 甲、乙、丙三种物质分别配制饱和溶液时,丙需要水的质量最大,因此所得饱和溶液质量最大的是丙.
(5)由溶解度曲线可知,甲、乙物质的溶解度随温度的升高而增大,饱和溶液在降低温度时能析出晶体,由于甲在两温度下的溶解度差值较大,所以降温析出晶体多;丙物质的溶解度随温度的升高而减少,饱和溶液在降低温度将变成不饱和溶液,不能析出晶体.
故答案为:
(1)在40℃时,物质甲和乙的溶解度相等;
(2)增加溶质(或蒸发溶剂或升高温度);
(3)冷却热饱和溶液;
(4)丙;
(5)甲.
点评 主要考查了固体溶解度曲线所表示的意义及固体溶解度和温度之间的关系,加强对溶解度的理解是正确解题的关键.

练习册系列答案
相关题目
19.下列说法中不正确的是( )
| A. | 用红磷测定空气中氧气含量时,红磷一定要过量 | |
| B. | 用排水法收集氧气时,导管口刚有气泡冒出就收集气体 | |
| C. | 硫粉在氧气中燃烧时,集气瓶中放少量水可吸收二氧化硫 | |
| D. | 铁丝在氧气中燃烧时,集气瓶中放少量水可防止瓶底炸裂 |
16.如图为某化学反应的微观示意图,图中“●”表示硫原子,“○”表示氧原子,下列说法中错误的是( )

| A. | 甲是SO2 | |
| B. | 该反应属于化合反应 | |
| C. | 反应中,甲、乙、丙三种物质的分子个数比为2:1:2 | |
| D. | 反应前后,分子、原子种类均不变 |
20.如图所示,这四位同学描述的可能是下面的同一个化学符号( )


| A. | CO2 | B. | O2 | C. | NO | D. | HClO |
1.如图所示实验基本操作正确的是( )
| A. |  将铁钉放入试管中 | B. | 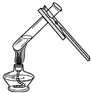 给试管内的液体加热 | ||
| C. | 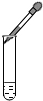 向试管内的滴加液体 | D. | 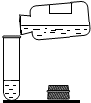 向试管中倾倒液体 |
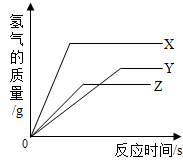 为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的同一种稀硫酸反应,都生成+2价金属的硫酸盐,反应情况如图所示.下列对该图象理解的叙述中,正确的是( )
为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的同一种稀硫酸反应,都生成+2价金属的硫酸盐,反应情况如图所示.下列对该图象理解的叙述中,正确的是( )