题目内容
10.下列叙述正确的是( )| A. | 锌、铁等金属能置换出酸中的氢气 | |
| B. | 用钢丝刷擦洗铝锅上的污垢 | |
| C. | 铁丝与硫酸铜溶液反应后溶液质量会减少 | |
| D. | 铝比铁的抗腐蚀能力强的原因是因为铁的化学性质比铝活泼 |
分析 A、根据锌铁等金属能转换出酸中的氢元素,而非氢气分析;
B、根据铝表面可以形成保护膜分析;
C、根据铁和硫酸铜溶液反应的方程式的意义分析;
D、根据铝和铁的活动性分析.
解答 解:A、锌铁等金属能转换出酸中的氢元素,而非氢气,故错误;
B、铝表面可以形成一层致密的氧化铝薄膜,起到保护作用,所以铝锅常用钢丝擦洗是错误的;
C、铁和硫酸铜反应的化学方程式及其质量关系为:Fe+CuSO4═FeSO4+Cu,
56 64
由以上可知,当有56份质量的铁反应形成溶液的一部分时,会有64份质量的铜从溶液中析出,充分反应后溶液的质量减小,故正确;
D、铝在空气中易被氧气氧化,表面形成致密的氧化铝保护膜,因此不易生锈,但铝的活动性比铁强,故错误;
故选项为:C.
点评 本题考查了金属的有关性质和应用,完成此题,可以依据已有的知识进行,能够考查学生的知识综合能力.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案
相关题目
5.如图是甲、乙两种固体物质的溶解度曲线,下列说法不正确的是( )


| A. | 甲、乙物质都是易溶物 | |
| B. | 当甲中混有少量乙时,可用冷却热饱和溶液的方法提纯甲 | |
| C. | 甲的饱和溶液从30℃降温至10℃后仍然饱和 | |
| D. | 10℃时,甲、乙的饱和溶液中所含溶质质量一定相等 |
2.下列物质的名称、俗名与化学式完全对应的是( )
| A. | 氯化钠 食盐 NaCl2 | B. | 碳酸氢钠 纯碱 NaHCO3 | ||
| C. | 氢氧化钙 熟石灰 CaO | D. | 氢氧化钠 烧碱 NaOH |
16.下列关于资源、能源、环保方面的叙述正确的是( )
| A. | 空气是一种宝贵的资源,其中含量最多的化合物是氮气 | |
| B. | 目前我国已使用可燃冰来代替化石燃料以解决空气污染问题 | |
| C. | 使用车用乙醇汽油不仅可以节约现有能源,而且可以杜绝温室效应 | |
| D. | 水污染加剧了水资源的短缺 |
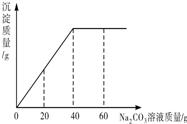 实验室有一瓶未知浓度的BaCl2溶液,某同学取出104g该溶液于烧杯中,向其中逐滴加入溶质质量分数为26.5%的Na2CO3溶液.反应过程中生成沉淀的质量与所用Na2CO3溶液质量的关系如图所示.已知:BaCl2+Na2CO3═BaCO3↓+2NaCl请计算:
实验室有一瓶未知浓度的BaCl2溶液,某同学取出104g该溶液于烧杯中,向其中逐滴加入溶质质量分数为26.5%的Na2CO3溶液.反应过程中生成沉淀的质量与所用Na2CO3溶液质量的关系如图所示.已知:BaCl2+Na2CO3═BaCO3↓+2NaCl请计算: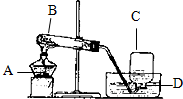 如图是实验室用高锰酸钾加热制取氧气的实验装置,请写出仪器名称:
如图是实验室用高锰酸钾加热制取氧气的实验装置,请写出仪器名称: