题目内容
15.向AgNO3、Cu(NO3)2的混合溶液中加入一定量的铝粉,充分反应后过滤,若向滤渣中滴加稀盐酸后有气泡冒出,则滤渣中含有的金属是铝,银和铜;若滤渣中无气泡生成,则滤液中一定含有的金属离子是Al3+(填离子符号).分析 根据金属银、铜、铝的活动性由强到弱的顺序铝>铜>银,当把铝粉加入到AgNO3、Cu(NO3)2的混合溶液中,首先置换出银,银被置换完才继续置换铜;根据向滤出的固体上滴加稀盐酸时有气泡产生,可判断铝粉有剩余;
解答 解:金属的活动性顺序:K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb(H)Cu、Hg、Ag、Pt、Au,故当把铝粉加入到AgNO3、Cu(NO3)2的混合溶液中,首先置换出银,银被置换完才继续置换铜;根据向滤出的固体上滴加稀盐酸时有气泡产生,可判断铝粉有剩余,因此在滤液中不可能再有硝酸银和硝酸铜,所以滤出的金属有过量的铝,被置换出的银和铜;根据“若滤渣中无气泡生成”,所以说明铝完全反应,而无法确定AgNO3、Cu( NO3)2中金属离子是否全置换出,但溶液中一定含有的金属阳离子是铝离子.
故答案为:铝,银和铜;Al3+;
点评 考虑金属与盐溶液反应,只有排在前面的金属才能把后面的金属从其盐溶液中置换出来,并且置换的先后顺序为由弱到强.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
10. 甲、乙两种固体溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体溶解度曲线如图所示,下列说法正确的是( )
 甲、乙两种固体溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体溶解度曲线如图所示,下列说法正确的是( )| A. | N点表示t2℃时甲溶液为饱和状态 | |
| B. | 降温或蒸发可使乙物质从其饱和溶液中结晶出来 | |
| C. | 甲、乙饱和溶液从t1℃到t2℃,其溶质质量分数均保持不变 | |
| D. | t1℃时,甲、乙饱和溶液中溶质和溶剂的质量比均为1:4 |
20.用双氧水制取氧气时,忘记加二氧化锰的后果是( )
| A. | 不放出氧气 | B. | 放出的氧气的速度慢 | ||
| C. | 放出的氧气的质量会减少 | D. | 放出的氧气的速度慢且质量会减少 |
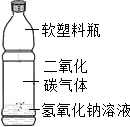 化学课堂上,同学们正在探究二氧化碳气体与碱溶液能否发生化学反应.
化学课堂上,同学们正在探究二氧化碳气体与碱溶液能否发生化学反应.