题目内容
12.发射卫星的火箭所用的燃料是肼(N2H4),推进剂是四氧化氮(N2O4),两者反应的化学方程式为:2N2H4+N2O4$\frac{\underline{\;点燃\;}}{\;}$3X+4H2O,则X的化学式是( )| A. | NO | B. | NO2 | C. | N2 | D. | HNO3 |
分析 由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
解答 解:由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式2N2H4+N2O4$\frac{\underline{\;点燃\;}}{\;}$3X+4H2O,反应前氮、氢、氧原子个数分别为6、8、4,反应后的生成物中氮、氢、氧原子个数分别为0、8、4,根据反应前后原子种类、数目不变,则3X分子中含有6个氮原子,则每个X分子由2个氮原子构成,则物质X的化学式为N2.
故选:C.
点评 本题难度不大,掌握利用化学反应前后原子守恒来确定物质的化学式的方法是正确解答此类题的关键.

练习册系列答案
相关题目
2.我国著名化学家侯德榜发明的联合制碱法的主要过程是:①向饱和的食盐水中通入氨气,制成饱和铵盐水;②在加压条件下向饱和铵盐水中通入二氧化碳,两者发生反应生成碳酸氢钠,有晶体析出;③将析出的碳酸氢钠加热制得碳酸钠、二氧化碳和水.四种盐在不同温度下的溶解度表:
请回答:(1)碳酸氢铵的化学式是NH4HCO3.
(2)由上表分析过程②中能发生反应的原因是在相同温度下碳酸氢钠的溶解度最小.
| 温度 溶解度/g 盐 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ |
| 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| 碳酸氢铵 | 15.8 | 21.0 | 27.0 | ------- | ------- |
| 碳酸氢钠 | 8.1 | 9.6 | 11.1 | 12.7 | ------- |
| 氯化铵 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
(2)由上表分析过程②中能发生反应的原因是在相同温度下碳酸氢钠的溶解度最小.
7.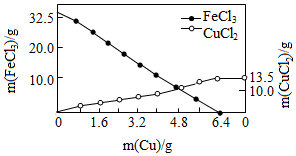 FeCl3溶液常用于蚀刻印刷电路,反应原理为aFeCl3+bCu═cCuCl2+dX.向含溶质32.5g的FeCl3溶液中慢慢加入一定量的Cu粉,反应过程中FeCl3、CuCl2的质量随Cu粉质量变化如图.下列说法不正确的是( )
FeCl3溶液常用于蚀刻印刷电路,反应原理为aFeCl3+bCu═cCuCl2+dX.向含溶质32.5g的FeCl3溶液中慢慢加入一定量的Cu粉,反应过程中FeCl3、CuCl2的质量随Cu粉质量变化如图.下列说法不正确的是( )
 FeCl3溶液常用于蚀刻印刷电路,反应原理为aFeCl3+bCu═cCuCl2+dX.向含溶质32.5g的FeCl3溶液中慢慢加入一定量的Cu粉,反应过程中FeCl3、CuCl2的质量随Cu粉质量变化如图.下列说法不正确的是( )
FeCl3溶液常用于蚀刻印刷电路,反应原理为aFeCl3+bCu═cCuCl2+dX.向含溶质32.5g的FeCl3溶液中慢慢加入一定量的Cu粉,反应过程中FeCl3、CuCl2的质量随Cu粉质量变化如图.下列说法不正确的是( )| A. | X为FeCl2 | B. | 化学计量数c=1 | ||
| C. | 方程式中a和b的比为1:2 | D. | 完全反应后,生成X的质量为25.4g |
17.物质的用途与性质密切相关,下列说法错误的是( )
| A. | 氮气常用作保护气,是由于氮气的化学性质不活泼 | |
| B. | 用金属铜制作电路板,是因为铜具有导电性 | |
| C. | 工业上常用稀硫酸除去铁锈,是由于稀硫酸能与铁反应 | |
| D. | 用一氧化碳冶炼金属,是由于一氧化碳具有还原性 |
4.汽车尾气净化装置中装有钡催化剂,下图是尾气在催化剂表面反应过程的微观示意图下列有关说法不正确的是( )


| A. | 化学反应前后原子种类、个数、质量均没有改变 | |
| B. | 反应Ⅱ的反应前后一共涉及三种分子 | |
| C. | 反应Ⅱ中参加反应的二氧化氮与一氧化碳的分子个数为1:2 | |
| D. | 此净化装置可以消除一氧化碳、一氧化氮、二氧化氮对空气的污染 |
1.人吸入的空气与呼出的气体相比,呼出的气体中明显增加的气体是( )
| A. | 氧气 | B. | 氧气和二氧化碳 | ||
| C. | 氮气 | D. | 二氧化碳和水蒸气 |
2.以下不属于溶液特征的是( )
| A. | 均一 | B. | 稳定 | C. | 无色 | D. | 透明 |