题目内容
10.硫酸是常见的酸,也是常用的化工原料.由于浓度不同,浓硫酸与稀硫酸在性质上存在较大差异,如浓硫酸具有脱水性、吸水性和强腐蚀性等.某课外兴趣小组为了探究浓硫酸的某些特性做了如下一些实验.请结合有关实验,按要求回答下列问题:(1)用玻璃棒蘸取少量浓硫酸在滤纸上写字,过后观察,字迹显黑色,这主要是由于浓硫酸具有脱水性,使纸中的纤维素炭化的缘故;在洗气瓶中盛放浓硫酸,除去氢气或氧气中的水分,是利用其吸水性.
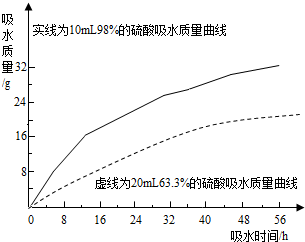
(2)探究浓硫酸的吸水性.兴趣小组把98%的硫酸10mL和63.3%的硫酸(用10mL98%的硫酸与10mL水配成)约20mL分别放入两个相同的大表面皿中,称量、观察、记录、分析.根据室温环境下实验的数据绘成的曲线如图:
①释浓硫酸时,应将浓硫酸沿着烧杯内壁缓缓地注入盛有水的烧杯中并不断搅拌.
②由如图曲线你能得到的实验结论有哪些?(写两点)浓硫酸和一定浓度以上的稀硫酸都具有吸水性、浓硫酸吸水能力比稀硫酸强(吸水速度快、吸水量大).
分析 (1)依据浓硫酸具有的脱水性与吸水性进行分析判断;
(2)①根据浓硫酸的稀释过程的操作要领分析解答;
②从曲线观察两种不同的酸的吸水情况的变化趋势分析解答.
解答 解:(1)浓硫酸具有的脱水性与吸水性,用玻璃棒蘸取少量浓硫酸在滤纸上写字,过后观察,字迹显黑色是因为其脱水性导致的纸张炭化,而除去氢气或氧气中的水分,是利用其吸水性,起到干燥剂的作用;
(2)①浓硫酸的稀释时应酸入水并不断搅拌使溶解时产生的热量尽快散失;
②从曲线观察两种不同的酸的吸水情况的变化可知:浓硫酸和一定浓度以上的稀硫酸都具有吸水性;浓硫酸吸水能力比稀硫酸强(吸水速度快、吸水量大);开始两者吸水速度差异比较大,随着时间的推移吸水速度越来越接近,吸水能力越来越弱;硫酸浓度越稀吸水性越弱,到一定浓度后就失去吸水性;硫酸吸水能力可能会受环境温度、湿度、气压、酸的用量、表面积等因素的影响等.
故答案为:
(1)脱水; 吸水;
(2)①浓硫酸,水; ②浓硫酸和一定浓度以上的稀硫酸都具有吸水性;浓硫酸吸水能力比稀硫酸强(吸水速度快、吸水量大).
点评 该题属于实验方案的探究题,主要是采用对比实验的方法对实验中的问题进行探讨,掌握设计实验的目的及方法是解题的关键所在.

练习册系列答案
相关题目
18.下列各组中的物质,能在溶液中大量共存的是( )
| A. | KOH Na2CO3 HCl | B. | KNO3 NaCl NaOH | ||
| C. | KNO3 NaOH FeCl3 | D. | AgNO3 BaCl2 HNO3 |
15.蔬菜、水果对人体可以起到调节新陈代谢、预防疾病和维持身体健康的作用,主要是因为蔬菜、水果中富含人体需要的( )
| A. | 油脂 | B. | 维生素 | C. | 蛋白质 | D. | 淀粉 |
2.有一包白色粉末可能含有硫酸钡、碳酸钾和氢氧化钡中的一种或几种,取一定量该粉末加入到盛有足量水的烧杯中,搅拌、静置,观察到烧杯中有白色不溶物.
友情提示:氯化钡溶液为中性.
(1)进一步确定白色固体成分,小明同学进行如下实验探究:
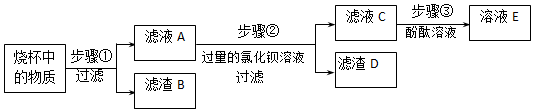
Ⅰ.步骤②中发生化学反应的方程式是K2CO3+BaCl2=BaCO3↓+2KCl;
Ⅱ.
(2)小军同学认为只需进行一步实验就能说明原白色粉末中三种物质都含有,则小军同学的实验
为:(操作和现象)在滤渣B中加入过量的稀硝酸,沉淀部分溶解.
友情提示:氯化钡溶液为中性.
(1)进一步确定白色固体成分,小明同学进行如下实验探究:

Ⅰ.步骤②中发生化学反应的方程式是K2CO3+BaCl2=BaCO3↓+2KCl;
Ⅱ.
| 实验操作 | 现象 | 结论 |
| 步骤③中,加入酚酞溶液 | 若溶液E为无色 | 原白色粉末的组成是硫酸钡、碳酸钾; |
| 若溶液E为红色 | 滤液A中一定含有的溶质是氢氧化钾, 原白色粉末的可能组成分别是碳酸钾和氢氧化钡或硫酸钡、碳酸钾和氢氧化钡. |
为:(操作和现象)在滤渣B中加入过量的稀硝酸,沉淀部分溶解.
19.以下初中阶段所学的相关化学知识,说法以及解释,其中正确的是( )
| 相关化学知识、说法 | 解释 | |
| A | 碳、硫与氧气反应是化合反应 | 氧气均支持这些物质燃烧 |
| B | 氧化钙和浓硫酸加入水都放热 | 二者均发生了化学变化 |
| C | 乙醇和甲烷都是有机物 | 二者均为含碳元素的化合物 |
| D | 稀硫酸、硫酸铜溶液显酸性 | 溶液中均含有硫酸根离子 |
| A. | A | B. | B | C. | C | D. | D |