题目内容
请根据下列装置回答有关问题:
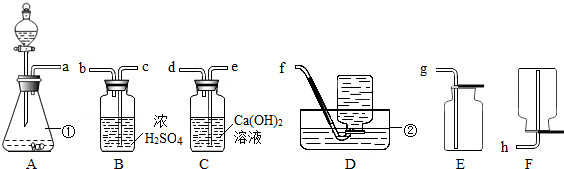
(1)写出图中标有①、②的仪器名称:①为 ;②为 .
(2)若用上述装置制取二氧化碳,则A中发生反应的化学方程式为 .要制取和收集一瓶干燥的二氧化碳气体,选用的装置有 (填字母代号),其装置接口的连接顺序是(用接口字母顺序从左至右连接) .
(3)利用上述气体发生装置制取氧气,则A中发生反应的化学方程式为 .现要配制100g溶质质量分数为6%的双氧水溶液,需要30%的双氧水溶液 g,需要加入水的体积为 mL.

(1)写出图中标有①、②的仪器名称:①为
(2)若用上述装置制取二氧化碳,则A中发生反应的化学方程式为
(3)利用上述气体发生装置制取氧气,则A中发生反应的化学方程式为
考点:常用气体的发生装置和收集装置与选取方法,气体的干燥(除水),实验室制取氧气的反应原理,二氧化碳的实验室制法,用水稀释改变浓度的方法,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:根据图示即可写出仪器的名称;碳酸钙能与盐酸反应生成氯化钙、水和二氧化碳,发生装置的选择要看反应物的状态和反应条件;收集装置的选择要看气体的密度和溶解性;配置溶液的计算方法,据此解答.
解答:解:(1)据图可知①是锥形瓶,②是水槽;
(2)碳酸钙能与盐酸反应生成氯化钙、水和二氧化碳;要制取和收集一瓶干燥的二氧化碳气体,使用浓硫酸进行干燥,长管进短管出,用向上排空气法收集,其装置为ABE;接口的连接顺序是a-c-b-g;
(3)利用上述气体发生装置制取氧气,为过氧化氢分解制取氧气,则A中发生反应的化学方程式为2H2O2
2H2O+O2↑;
根据稀释前后过氧化氢的质量前后保持不变,设需要30%的双氧水的质量为x,依据计算公式可得:
100g×6%=30%x,
则 x=20g; 需要水的质量为:100g-20g=80g即80mL;
故答案为:(1)①锥形瓶,②水槽;(2)ABE,a-c-b-g;(3)2H2O2
2H2O+O2↑;20,80.
(2)碳酸钙能与盐酸反应生成氯化钙、水和二氧化碳;要制取和收集一瓶干燥的二氧化碳气体,使用浓硫酸进行干燥,长管进短管出,用向上排空气法收集,其装置为ABE;接口的连接顺序是a-c-b-g;
(3)利用上述气体发生装置制取氧气,为过氧化氢分解制取氧气,则A中发生反应的化学方程式为2H2O2
| ||
根据稀释前后过氧化氢的质量前后保持不变,设需要30%的双氧水的质量为x,依据计算公式可得:
100g×6%=30%x,
则 x=20g; 需要水的质量为:100g-20g=80g即80mL;
故答案为:(1)①锥形瓶,②水槽;(2)ABE,a-c-b-g;(3)2H2O2
| ||
点评:本题考查了常见气体的实验室制取,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
检验久未开启的菜窖内二氧化碳的浓度是否过大的正确方法是( )
| A、带入一个盛满澄清石灰水的试管 |
| B、带入一杯水 |
| C、带入一阁接通电源的电筒 |
| D、带入一盏点燃的油灯或木柴 |
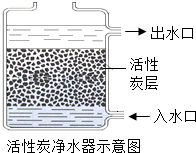 水是生命的源泉,也是不可缺少的资源.
水是生命的源泉,也是不可缺少的资源.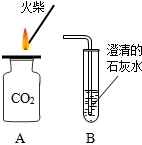 右图所示中表示二氧化碳气验满的操作的是
右图所示中表示二氧化碳气验满的操作的是