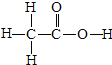题目内容
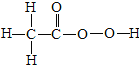
2013年3月底,上海、浙江一带出现H7N9禽流感.这种病毒首先在鸡、鸭等飞禽身上发现.对鸡、鸭舍进行消毒时常用15%的过氧乙酸溶液,过氧乙酸的化学式是CH3COOOH(即:C2H4O3).试计算:
(1)一个过氧乙酸分子中有 个原子.
(2)过氧乙酸中碳、氢、氧元素的质量比 .
(3)过氧乙酸中氧元素的质量分数是 .(精确到0.1%)
(4)配制15%的过氧乙酸溶液100克,需过氧乙酸 克,水 mL.(ρ水=1g/cm3)
(1)一个过氧乙酸分子中有
(2)过氧乙酸中碳、氢、氧元素的质量比
(3)过氧乙酸中氧元素的质量分数是
(4)配制15%的过氧乙酸溶液100克,需过氧乙酸
考点:元素质量比的计算,有关溶质质量分数的简单计算,元素的质量分数计算
专题:化学式的计算,溶液的组成及溶质质量分数的计算
分析:(1)根据一个过氧乙酸分子的构成进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中某元素的质量分数=
×100%
(4)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得水的质量.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中某元素的质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
(4)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得水的质量.
解答:解:(1)一个过氧乙酸分子是由2个碳原子、4个氢原子和3个氧原子构成的,则每个过氧乙酸分子中含有9个原子.
(2)过氧乙酸中碳、氢、氧元素的质量比为(12×2):(1×4):(16×3)=6:1:12.
(3)过氧乙酸中氧元素质量分数为
×100%=62.3%
(4)配制15%的过氧乙酸溶液100克,需过氧乙酸的质量为100g×15%=15g,需要水的质量为:100g-15g=85g,其体积为
=85cm3=85mL.
故答案为:(1)9;(2)6:1:12;(3)62.3%;(4)15;85.
(2)过氧乙酸中碳、氢、氧元素的质量比为(12×2):(1×4):(16×3)=6:1:12.
(3)过氧乙酸中氧元素质量分数为
| 16×3 |
| 12×2+1×4+16×3 |
(4)配制15%的过氧乙酸溶液100克,需过氧乙酸的质量为100g×15%=15g,需要水的质量为:100g-15g=85g,其体积为
| 85g |
| 1g/mL |
故答案为:(1)9;(2)6:1:12;(3)62.3%;(4)15;85.
点评:本题难度不大,考查同学们结合新信息、灵活运用化学式与溶质质量分数的关计算进行分析问题、解决问题的能力.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
如图所示的家庭小实验中,主要发生化学变化的是( )
A、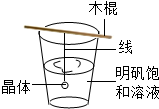 制取明矾晶体 |
B、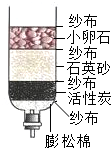 自制净水器净水 |
C、 自制“叶脉书签” |
D、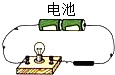 石墨导电实验 |