题目内容
2.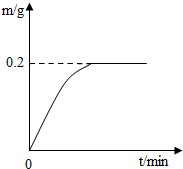 日常生活中接触的金属材料,大多属于合金.其中黄铜是以锌作主要添加元素的铜合金.已知组成某弹壳的黄铜中只含有锌和铜,现将22g该弹壳碾成粉末后放入盛有足量的稀硫酸烧杯中,测得反应过程中生成的氢气的质量(单位为g)与反应时间(单位为min)的关系如图所示.试计算:
日常生活中接触的金属材料,大多属于合金.其中黄铜是以锌作主要添加元素的铜合金.已知组成某弹壳的黄铜中只含有锌和铜,现将22g该弹壳碾成粉末后放入盛有足量的稀硫酸烧杯中,测得反应过程中生成的氢气的质量(单位为g)与反应时间(单位为min)的关系如图所示.试计算:(1)由题意可知,反应生成氢气的质量共0.2g;
(2)弹壳中铜的质量(精确至0.1)
(3)若欲计算反应后所得溶液的质量,你认为至少还应该补充的一个条件是稀硫酸的质量.
分析 (1)根据图中的信息可知氢气的质量;
(2)铜与稀硫酸不反应.利用锌与硫酸反应的化学方程式,根据氢气的质量求出锌的质量,进而求出黄铜中铜的质量;
(3)根据溶质的质量分数计算公式分析回答.
解答 解:
(1)根据题意可知,生成氢气的质量为0.2g
(2)设黄铜中锌的质量为x
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.2g
$\frac{65}{x}=\frac{2}{0.2g}$
x=6.5g
弹壳中铜的质量为:22g-6.5g=15.5g
(3)若要计算反应后所得溶液中ZnSO4的质量分数,根据锌与硫酸反应的方程式可计算出硫酸锌的质量,还应知道溶液的质量,所以,至少还应该补充的一个条件是稀硫酸的质量.
答案:
(1)0.2g;
(2)原样品中铜的质量为15.5g;
(3)稀硫酸的质量.
点评 本题考查根据化学方程式的简单计算,已知生成物的质量求反应物的质量,解题的关键是正确的对图象意义的分析;

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目
7.某化学兴趣小组的同学做了如图所示两个实验.下列有关说法正确的是( )
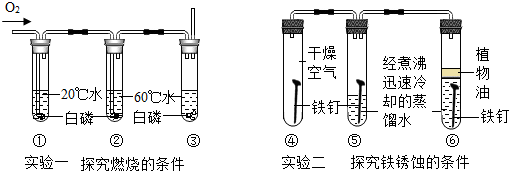

| A. | ①、②号试管中的白磷都不能燃烧 | |
| B. | 久置后,④、⑥号试管中的铁钉都不生锈 | |
| C. | ②、③号试管控制的变量是氧气 | |
| D. | ⑤、⑥号试管中铁钉都没有与氧气接触 |
14. 2014年科学家用钙(Ca)原子轰击锫(Bk)原子,确定合成了117号元素(部分信息如图所示),填补了元素周期表最后一个空格.下列说法错误的是( )
2014年科学家用钙(Ca)原子轰击锫(Bk)原子,确定合成了117号元素(部分信息如图所示),填补了元素周期表最后一个空格.下列说法错误的是( )
 2014年科学家用钙(Ca)原子轰击锫(Bk)原子,确定合成了117号元素(部分信息如图所示),填补了元素周期表最后一个空格.下列说法错误的是( )
2014年科学家用钙(Ca)原子轰击锫(Bk)原子,确定合成了117号元素(部分信息如图所示),填补了元素周期表最后一个空格.下列说法错误的是( )| A. | 该元素原子的核外电子数为117 | B. | 该元素的原子序数为117 | ||
| C. | 该元素的相对原子质量为294g | D. | 钙和锫都属于金属元素 |
12.属于纯净物的是( )
| A. | 空气 | B. | 石灰水 | C. | 蒸馏水 | D. | 天然气 |

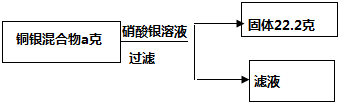 向铜银混合物中,加入溶质质量分数为10%的硝酸银溶液340g,恰好完全反应,请结合图提供的数据计算.求:
向铜银混合物中,加入溶质质量分数为10%的硝酸银溶液340g,恰好完全反应,请结合图提供的数据计算.求: