题目内容
15.甲同学取40g氧化铜与100g稀硫酸恰好完全反应,反应后得一种蓝色溶液.(1)甲同学所得蓝色溶液中溶质的化学式为CuSO4.
(2)试计算稀硫酸中溶质的质量分数,写出计算过程.
分析 氧化铜和稀硫酸反应生成硫酸铜和水,根据氧化铜的质量可以计算反应的硫酸的质量和生成的硫酸铜的质量,进一步可以计算稀硫酸中溶质的质量分数.
解答 解:(1)氧化铜和稀硫酸反应生成硫酸铜和水,甲同学所得蓝色溶液中溶质为硫酸铜;答案:CuSO4;
(2)设硫酸的质量为x,
CuO+H2SO4═CuSO4+H2O,
80 98
40g x
$\frac{80}{40g}=\frac{98}{x}$,
x=49g,
稀硫酸中溶质的质量分数为:$\frac{49g}{100g}$×100%=49%,
答:稀硫酸中溶质的质量分数为49%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
5.有一杯食盐水,若上部的密度是bg/cm3,则下部的密度是( )
| A. | 大于b g/cm3 | B. | 无法判断 | C. | 小于b g/cm3 | D. | 等于b g/cm3 |
6.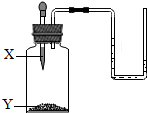 如图所示装置,将X滴加到固体Y中,U形管中的液面变得右高左低,则X、Y对应的试剂组是C
如图所示装置,将X滴加到固体Y中,U形管中的液面变得右高左低,则X、Y对应的试剂组是C
 如图所示装置,将X滴加到固体Y中,U形管中的液面变得右高左低,则X、Y对应的试剂组是C
如图所示装置,将X滴加到固体Y中,U形管中的液面变得右高左低,则X、Y对应的试剂组是C选项 试剂 | A | B | C | D |
| X | H2O | H2O | H2O | H2O2 |
| Y | NaCl | NH4NO3 | NaOH | MnO2 |
3. 如图是元素周期表的部分,其中碳元素部分信息缺失,下列有关该元素认识错误的是( )
如图是元素周期表的部分,其中碳元素部分信息缺失,下列有关该元素认识错误的是( )
 如图是元素周期表的部分,其中碳元素部分信息缺失,下列有关该元素认识错误的是( )
如图是元素周期表的部分,其中碳元素部分信息缺失,下列有关该元素认识错误的是( )| A. | 该元素对应原子的质子数为6 | |
| B. | 该元素属于金属元素 | |
| C. | 该元素可以组成多种单质 | |
| D. | 该元素化学性质与最外层电子数密切相关 |
7.下列变化属于物理变化的是( )
| A. | 冰山融化 | B. | 白磷自燃 | C. | 牛奶变质 | D. | 植物光合作用 |
5.MnO2中Mn元素的化合价为( )
| A. | -2 | B. | -4 | C. | +4 | D. | +2 |
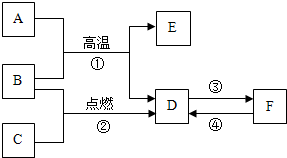 如图所示:A~F是初中化学常见的物质.在常温下,A为黑色固体,E为红色固体单质,B、C、D均为无色气体,且D能使澄清的石灰水变浑浊,F为常用建筑材料的主要成分.
如图所示:A~F是初中化学常见的物质.在常温下,A为黑色固体,E为红色固体单质,B、C、D均为无色气体,且D能使澄清的石灰水变浑浊,F为常用建筑材料的主要成分.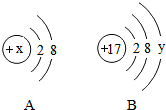 如图中A、B分别是某微粒的结构示意图,回答下列问题:
如图中A、B分别是某微粒的结构示意图,回答下列问题: