题目内容
2.在一个密闭容器里有A、B、C、D四种物质,在一定的条件下充分反应,测得反应前后各物质的质量如图表,下列说法中正确的是( )| 物质 | A | B | C | D |
| 反应前的质量/g | 4 | 6 | 111 | 4 |
| 反应后的质量/g | 待测 | 15 | 0 | 84 |
| A. | 反应后密闭容器中A的质量为22g | |
| B. | 密闭容器中发生的化学反应属于化合反应 | |
| C. | 该反应中A、B、C、D四种物质的质量比为22:9:111:90 | |
| D. | 密闭容器中发生的化学反应属于分解反应 |
分析 B的质量增大15g-6g=9g,D的质量增大84g-4g=80g,则B、D为生成物,C的质量减少111g,C为反应物,由于111g>9g+80g=89g,故A为生成物,根据质量守恒定律可以计算生成A的质量,可得反应后A的总质量.
解答 解:B的质量增大15g-6g=9g,D的质量增大84g-4g=80g,则B、D为生成物,C的质量减少111g,C为反应物,由于111g>9g+80g=89g,故A为生成物;
A、根据质量守恒定律,生成A的质量为111g-89g=22g,则反应后,待测A的质量为4g+22g=26 g,错误;
B、该反应中反应物为C,生成物为A、B、D,一种物质反应生成三种物质,属于分解反应,错误;
C、该反应中A、B、C、D四种物质的质量比为22:9:111:80,错误;
D、该反应中反应物为C,生成物为A、B、D,一种物质反应生成三种物质,属于分解反应,正确;
故选D
点评 本题考查化学方程式计算,涉及质量守恒定律的应用,比较基础,注意从宏观的质量角度与微观原子角度理解质量守恒定律.

练习册系列答案
相关题目
14.如表所示实验方案合理的是( )
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 实验室制取CO2 | 块状大理石与稀硫酸 |
| B | 鉴别硬水和软水 | 观察液体是否浑浊 |
| C | 鉴别H2O、KCl溶液 | AgNO3溶液 |
| D | 除去CO2中少量的CO | 通入O2,点燃 |
| A. | A | B. | B | C. | C | D. | D |
12.有关物质的用途错误的是( )
| A. | 氧气--做燃料 | B. | 稀有气体--制作霓虹灯 | ||
| C. | 钛合金--做眼镜架 | D. | 干冰--做冷冻食品的制冷剂 |

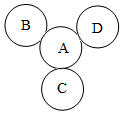 A、B、C、D是我们学过的初中常见的四种物质,分别用圆表示,两圆相切表示两种物质能够发生反应,A是无色无味气体,B是银白色金属,不能再空气中燃烧,但能在A中燃烧;C与A反应生成一种有刺激性气味的气体E,D在A中燃烧生成能使澄清石灰水变浑浊的气体,根据以上信息回答下列问题:
A、B、C、D是我们学过的初中常见的四种物质,分别用圆表示,两圆相切表示两种物质能够发生反应,A是无色无味气体,B是银白色金属,不能再空气中燃烧,但能在A中燃烧;C与A反应生成一种有刺激性气味的气体E,D在A中燃烧生成能使澄清石灰水变浑浊的气体,根据以上信息回答下列问题:
