题目内容
13.氢气、一氧化碳、二氧化碳和甲烷都是初中科学常见的气体.(1)可燃性气体与空气混合点燃可能会爆炸,所以可燃性气体点燃前应先检验气体的纯度
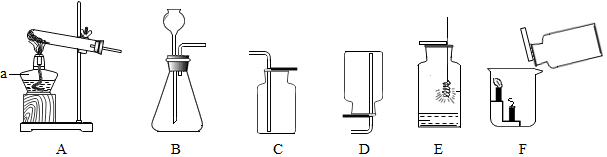
(2)某无色气体X可能含有氢气、一氧化碳、二氧化碳和甲烷四种气体中的一种或两种.为确认其组成某同学取一定量该气体按如图所示装置进行实验(假设每步都充分反应或吸收)

①同学们设计了装置②,其作用是吸收气体中的水分和二氧化碳
②装置③、④中盛放的试剂依次是ba(填序号)
a.烧碱溶液 b.浓硫酸
③取一定量该气体进行实验,发现装置①中无明显变化,装置③增重1.8g,装置④增重2.2g.则气体X的可能组成是CH4;H2和CO;CH4、H2、CO.
分析 (1)根据点燃可燃性气体容易发生爆炸考虑;
(2)①根据资料:NaOH固体易吸收水蒸气,据此分析装置B的作用即可.
②先经过NaOH溶液时会带水蒸气到浓硫酸中,影响测定结果,据此进行分析判断.
③装置A中无明显变化,排除了CO2;装置C增重1.8g,生成了1.8g水;装置D增重2.2 g,生成了2.2g二氧化碳;据此可以计算出所含氢元素、碳元素的质量,进而可以确定气体X的组成.
解答 解:(1)可燃性气体与空气混合点燃可能会爆炸,所以可燃性气体点燃前应先检验气体的纯度;
(2)①装置②中药品是固体NaOH和氯化钙,可作干燥剂,能吸收气体中的水分和二氧化碳,防止气体中水蒸汽和二氧化碳干扰实验.
②装置③盛放的试剂应为浓硫酸,目的是通过是否增重测定H元素的有无,装置④中盛放的试剂是烧碱溶液,目的是通过是否增重测定C元素的有无.先经过NaOH溶液时会带出水蒸气到浓硫酸中,影响水的测定结果.
③装置①中无明显变化,气体中不含CO2;装置C增重1.8 g,含H元素的质量为1.8g×$\frac{1×2}{18}$×100%=0.2g;装置D增重2.2 g,同理可知含C元素0.6g;气体X中含H元素0.2g、含C元素0.6g,碳元素和氢元素的原子个数比是:$\frac{0.6}{12}$:$\frac{0.2}{1}$=1:4,而甲烷中碳和氢的个数比是1:4,所以气体可能是甲烷,如果没有甲烷,是氢气和一氧化碳的混合物也可以,只要能保证碳和氢的个数比是1:4就行,还有一种可能就是既有甲烷也含有氢气和一氧化碳;所以气体的组成可能有:CH4;H2和CO;CH4、H2、CO.
故答案为:(1)检验气体的纯度;(2)①吸收气体中的水分和二氧化碳;②ba;③CH4;H2和CO;CH4、H2、CO.
点评 本题难度较大,涉及知识面广,对学生思维能力要求高,既考查知识的识记、理解、迁移、运用,又考查分析、对比、归纳等思维能力.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
| A. | 减少 | B. | 增加 | C. | 不变 | D. | 先增加后减少 |
| A. | Mg和Al | B. | Al和Cu | C. | Cu和Ag | D. | Mg和Ag |
| 物质 | M | N | X | Y |
| 反应前/g | 2 | 20 | 34 | 0 |
| 反应后/g | 2 | 38 | 0 | 16 |
| A. | 该反应属于分解反应 | B. | 该反应属于化合反应 | ||
| C. | 该反应生成的N、Y的质量比为9:8 | D. | M在反应中可能作催化剂 |
| A. | 一定有水蒸气 | B. | 一定有CO2 | C. | 一定没有CO2 | D. | 一定有H2和CO |
 2017年3月,“以国为重的大国工匠”徐立平的先进事迹受到广泛关注.“大国工匠”徐立平的工作是给固体燃料发动机的推进剂药面“动刀”整形,以满足火箭及导弹飞行的各种复杂需要.
2017年3月,“以国为重的大国工匠”徐立平的先进事迹受到广泛关注.“大国工匠”徐立平的工作是给固体燃料发动机的推进剂药面“动刀”整形,以满足火箭及导弹飞行的各种复杂需要.