题目内容
17.在实验室中,下列做法不可行的是( )| A. | 实验室剩余的药品不要随意丢弃,可拿回家继续做家庭实验 | |
| B. | 实验完毕,要及时洗净器皿,整理好实验用品,擦净桌面 | |
| C. | 实验中浓硫酸不慎沾到手上,应立即用水冲洗 | |
| D. | 将实验室制氧气后的废液经静置、过滤、晾干后可回收二氧化锰固体 |
分析 A、根据实验室剩余药品的处理原则,进行分析判断.
B、根据实验完毕后应整理实验台,进行分析判断.
C、根据浓硫酸不慎沾到皮肤上的处理方法,进行分析判断.
D、实验室制氧气后的废液中含有水、二氧化锰,二氧化锰难溶于水,据此进行分析判断.
解答 解:A、实验室剩余的药品,既不能放回原瓶,也不可随意丢弃,更不能带出实验室,应放入的指定的容器内,故选项说法错误.
B、实验完毕,要及时洗净器皿,整理好实验用品,擦净桌面,故选项说法正确.
C、浓硫酸具有较强的腐蚀性,实验中浓硫酸不慎沾到手上,应立即用大量清水冲洗,若需要,再涂上3%~5%的碳酸氢钠溶液,故选项说法正确.
D、实验室制氧气后的废液中含有水、二氧化锰,二氧化锰难溶于水,可静置、过滤、晾干后可回收二氧化锰固体,故选项说法正确.
故选:A.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
相关题目
7.下表中,除去物质中所含少量杂质的方法和反应类型归类均正确的是( )
| 选项 | 物质 | 所含杂质 | 除去方法 | 反应类型 |
| A | CuO粉 | Cu粉 | 在空气中加热 | 化合反应 |
| B | H2 | HCl | 通过盛氢氧化钠溶液的洗气瓶 | 分解反应 |
| C | CO2 | CO | 通过灼热的CuO | 置换反应 |
| D | NaCl | Na2SO4 | 溶解,加过量的氯化钡溶液,并过滤 | 复分解反应 |
| A. | A | B. | B | C. | C | D. | D |
8.如图是甲、乙两种固体物质的溶解度曲线图.下列说法中正确的是( )
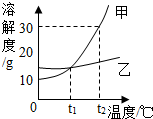

| A. | 甲的溶解度大于乙的溶解度 | |
| B. | 可采用降温的方法使甲物质的不饱和溶液变为饱和溶液 | |
| C. | t1℃时,甲、乙两种物质溶液的溶质质量分数相等 | |
| D. | t2℃时将30g甲物质放入50g水中,得到溶液的质量为80g |
2.鉴别下列物质的方法不合理的是( )
| 选 项 | 物 质 | 鉴别方法 |
| A | NaCl溶液和NaOH溶液 | 滴加稀盐酸,观察现象 |
| B | 氧气和二氧化碳 | 用燃烧的木条检验,观察现象 |
| C | 铝片和银片 | 分别加入到稀盐酸中,观察现象 |
| D | NaCl固体和NH4HCO3固体 | 加热 |
| A. | A | B. | B | C. | C | D. | D |
9. 衣食住行离不开化学.
衣食住行离不开化学.
(1)健康饮食需要营养素的合理搭配.下表为某品牌豆浆营养素标签的部分内容,请根据表中信息回答问题.
该豆浆含有六大营养素中的6种,其中能为人体提供能量的是糖类、脂肪、蛋白质;
(2)我国的汽车工业飞速发展,汽车数量剧增带来能源和环境双重问题.
①材料的开发和利用是汽车工业发展的基础,下列汽车配件材料中,属于合成有机高分子材料的是AE(填字母,下同)
A.合成橡胶轮胎 B.合金外壳 C.玻璃风挡
D.真皮座套 E.塑料内件
②一般汽车所用燃料为汽油或柴油,在汽油中添加乙醇(C2H5OH)制成乙醇汽油能一定程度上缓解能源危机,减少有害物质的排放,乙醇汽油属于混合物;乙醇在空气中燃烧的化学方程式为C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
(3)餐具上的油污可以用加入洗涤剂的水洗掉,说明洗涤剂具有乳化功能.
(4)下列物质中,能用来改良酸性土壤的物质是C(填序号).
A.盐酸 B.碳酸钠 C.氢氧化钙 D.氢氧化钠.
 衣食住行离不开化学.
衣食住行离不开化学.(1)健康饮食需要营养素的合理搭配.下表为某品牌豆浆营养素标签的部分内容,请根据表中信息回答问题.
| 成分 | 蛋白质 | 脂肪 | 糖类 | 钙 | 磷 | 铁 | 维生素A |
| 含量/100g | 1.8 | 0.7 | 1.1 | 0.01 | 0.03 | 0.0005 | 0.015 |
(2)我国的汽车工业飞速发展,汽车数量剧增带来能源和环境双重问题.
①材料的开发和利用是汽车工业发展的基础,下列汽车配件材料中,属于合成有机高分子材料的是AE(填字母,下同)
A.合成橡胶轮胎 B.合金外壳 C.玻璃风挡
D.真皮座套 E.塑料内件
②一般汽车所用燃料为汽油或柴油,在汽油中添加乙醇(C2H5OH)制成乙醇汽油能一定程度上缓解能源危机,减少有害物质的排放,乙醇汽油属于混合物;乙醇在空气中燃烧的化学方程式为C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
(3)餐具上的油污可以用加入洗涤剂的水洗掉,说明洗涤剂具有乳化功能.
(4)下列物质中,能用来改良酸性土壤的物质是C(填序号).
A.盐酸 B.碳酸钠 C.氢氧化钙 D.氢氧化钠.
6.下列变化中,属于化学变化的是( )
| A. | 莱阳梨榨汁 | B. | 蓬莱海市蜃楼 | C. | 张裕葡萄酿酒 | D. | 招远沙里淘金 |
7. 学完中和反应的知识后,某化学兴趣小组的同学在老师的指导下,对酸碱反应过程,溶液温度变化及如何判断酸碱溶液恰好完全反应进行了进一步的探究,请你参与.
学完中和反应的知识后,某化学兴趣小组的同学在老师的指导下,对酸碱反应过程,溶液温度变化及如何判断酸碱溶液恰好完全反应进行了进一步的探究,请你参与.
【探究活动一】酸碱反应过程中溶液的温度变化室温下,取10份相同体积100%NaOH溶液于10支试管中,分别滴加一定体积10%盐酸,并测定溶液温度的最高值.记录数据如下:
(1)写出氢氧化钠与盐酸反应的化学方程式NaOH+HCl═NaCl+H2O.
(2)由溶液温度的变化可知,氢氧化钠与盐酸反应放出(选填“放出”或“吸收”)热量.
(3)从实验记录的数据看,氢氧化钠完全反应时,加入盐酸的体积是在8-12mL(填体积范围)之间的某一数值;当加盐酸的体积在12-20mL之间,溶液温度下降,其原因之一是自然冷却.
【探究活动二】如何判断盐酸与氢氧化钠溶液恰好完全反应
(4)甲同学提出:可用酸碱指示剂进行判断.
根据化学实验中“反应现象必须明显”的设计原则:你认为要判断酸碱溶液恰好完全反应,应该选用酚酞(选填“石蕊”或“酚酞”)试液作指示剂.
具体的操作是:往滴有酚酞试液的氢氧化钠溶液逐滴加入盐酸溶液,溶液由红色逐渐变成无色.
(5)乙同学提出:可通过测定实验过程中溶液酸碱度的变化进行判断.
如图是某同学通过多次测定溶液的pH,画出的曲线,请你回答:
①该实验是将氢氧化钠溶液滴加到另一溶液中,图中a点表示当加入溶液的体积为V2时,pH=7,说明盐酸与氢氧化钠恰好完全反应,溶液呈中性.
②当加入溶液的体积为V1mL时,溶液中所含的溶质有NaCl和HCl(填化学式);
③滴加的NaOH溶液体积为V3mL时,溶液的pH大于7(选填“小于”、“等于”或“大于”).
 学完中和反应的知识后,某化学兴趣小组的同学在老师的指导下,对酸碱反应过程,溶液温度变化及如何判断酸碱溶液恰好完全反应进行了进一步的探究,请你参与.
学完中和反应的知识后,某化学兴趣小组的同学在老师的指导下,对酸碱反应过程,溶液温度变化及如何判断酸碱溶液恰好完全反应进行了进一步的探究,请你参与.【探究活动一】酸碱反应过程中溶液的温度变化室温下,取10份相同体积100%NaOH溶液于10支试管中,分别滴加一定体积10%盐酸,并测定溶液温度的最高值.记录数据如下:
| 加入盐酸体积/mL | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
| 测得溶液温度/℃ | 25.2 | 28.6 | 32.0 | 36.0 | 38.2 | 36.7 | 35.7 | 34.7 | 33.7 | 32.9 |
(2)由溶液温度的变化可知,氢氧化钠与盐酸反应放出(选填“放出”或“吸收”)热量.
(3)从实验记录的数据看,氢氧化钠完全反应时,加入盐酸的体积是在8-12mL(填体积范围)之间的某一数值;当加盐酸的体积在12-20mL之间,溶液温度下降,其原因之一是自然冷却.
【探究活动二】如何判断盐酸与氢氧化钠溶液恰好完全反应
(4)甲同学提出:可用酸碱指示剂进行判断.
根据化学实验中“反应现象必须明显”的设计原则:你认为要判断酸碱溶液恰好完全反应,应该选用酚酞(选填“石蕊”或“酚酞”)试液作指示剂.
具体的操作是:往滴有酚酞试液的氢氧化钠溶液逐滴加入盐酸溶液,溶液由红色逐渐变成无色.
(5)乙同学提出:可通过测定实验过程中溶液酸碱度的变化进行判断.
如图是某同学通过多次测定溶液的pH,画出的曲线,请你回答:
①该实验是将氢氧化钠溶液滴加到另一溶液中,图中a点表示当加入溶液的体积为V2时,pH=7,说明盐酸与氢氧化钠恰好完全反应,溶液呈中性.
②当加入溶液的体积为V1mL时,溶液中所含的溶质有NaCl和HCl(填化学式);
③滴加的NaOH溶液体积为V3mL时,溶液的pH大于7(选填“小于”、“等于”或“大于”).