题目内容
19.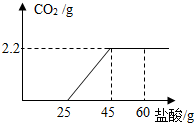 某氢氧化钙粉末中含有碳酸钙杂质.现取样品15g于锥形瓶中并加适量水搅拌得悬浊液,然后向锥形瓶中滴加稀盐酸,充分反应,测得加入稀盐酸的质量与反应生成气体的质量关系如图所示.
某氢氧化钙粉末中含有碳酸钙杂质.现取样品15g于锥形瓶中并加适量水搅拌得悬浊液,然后向锥形瓶中滴加稀盐酸,充分反应,测得加入稀盐酸的质量与反应生成气体的质量关系如图所示.(1)生成二氧化碳的质量是2.2g;
(2)加入60g稀盐酸后所得溶液中含有的溶质是CaCl2、HCl(填化学式);
(3)计算样品中碳酸钙的质量分数(写出计算过程,结果精确到0.1%).
分析 (1)由题目中图可以看出:当加入稀盐酸的质量为45g时,石灰石中的碳酸钙完全反应且生成二氧化碳的质量为2.2g.
(2)由图示可知,加入60g稀盐酸后盐酸过量,故溶液中含有的溶质是氯化钙和氯化氢;
(3)根据二氧化碳的质量,利用化学方程式,通过计算可求得样品中碳酸钙的质量分数.
解答 解:(1)由题目中图可以看出:当加入稀盐酸的质量为45g时,石灰石中的碳酸钙完全反应且生成二氧化碳的质量为2.2g;故答案为:2.2;
(2)由图示可知,加入60g稀盐酸后盐酸过量,故溶液中含有的溶质是氯化钙和氯化氢;故答案为:CaCl2;HCl;
(3)设样品中碳酸钙的质量分数为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
15g×x 2.2g
$\frac{100}{15gx}=\frac{44}{2.2g}$
解之得:
x=33.3%
答:样品中碳酸钙的质量分数为33.3%.
点评 本题是利用图表的方式来给出必要的数据并利用这些数据得出正确的答案,要求学生有较强的识图能力和数据分析能力.

练习册系列答案
相关题目
7.下列有关说法正确的是( )
| A. | 通过焚烧塑料减少“白色污染” | |
| B. | 可以用熟石灰来改良酸性土壤 | |
| C. | 煤燃烧产生大量的二氧化碳是造成酸雨的罪魁祸首 | |
| D. | 用一氧化碳做燃料可防止温室效应进一步增强 |
4.化学是材料科学、生命科学、环境科学和能源科学的重要基础.下列说法正确的是( )
| A. | 合金、合成纤维、合成橡胶都是有机合成材料 | |
| B. | 酒精、吗啡、海洛因都是毒品 | |
| C. | 二氧化硫、二氧化氮、粉尘都是大气污染物 | |
| D. | 石油、煤、氢气都是不可再生的化石燃料 |
11.下列变化中,属于化学变化的是( )
| A. | 胆矾研碎 | B. | 木炭燃烧 | C. | 石蜡熔化 | D. | 衣服晾干 |
8.复方篙甲醚(C16H26O5)是一种治疗疟疾的有效药品.下列说法正确的是( )
| A. | 复方篙甲醚属于有机物 | |
| B. | 复方篙甲醚由47个原子构成 | |
| C. | 复方篙甲醚的相对分子质量为298g | |
| D. | 复方篙甲醚中C、H、O三种元素的质量比是16:26:5 |
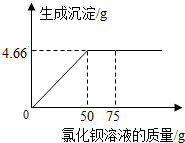 将4g含有可溶性杂质的硫酸铜样品溶于足量水,再向所得溶液中逐渐滴加75g一定溶质质量分数的氯化钡溶液(杂质不与氯化钡溶液反应),实验过程中,生成沉淀的质量与滴入氯化钡溶液的质量关系如图所示.试计算:
将4g含有可溶性杂质的硫酸铜样品溶于足量水,再向所得溶液中逐渐滴加75g一定溶质质量分数的氯化钡溶液(杂质不与氯化钡溶液反应),实验过程中,生成沉淀的质量与滴入氯化钡溶液的质量关系如图所示.试计算: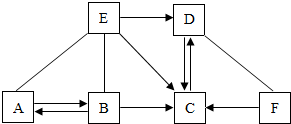 已知A、B、C、D、E分别分别是初中化学常见的五种不同类别的物质,其中B的固体和E的浓溶液常用作实验室的干燥剂.F是常见的一种棕色物质.它们之间存在如图所示的关系(图中“-”表示两端的物质能反应,“→”表示物质间存在转化关系,部分物质和反应条件示标出).请按要求回答下列问题:
已知A、B、C、D、E分别分别是初中化学常见的五种不同类别的物质,其中B的固体和E的浓溶液常用作实验室的干燥剂.F是常见的一种棕色物质.它们之间存在如图所示的关系(图中“-”表示两端的物质能反应,“→”表示物质间存在转化关系,部分物质和反应条件示标出).请按要求回答下列问题: