题目内容
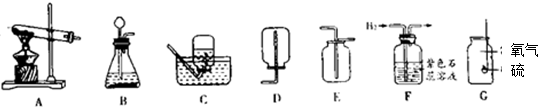
10.查资料显示,过氧化钠(Na2O2)和二氧化碳反应生成碳酸钠和氧气,化学方程式2Na2O2+2CO2=2Na2CO3+O2.小翔同学和小何同学分别设计了图甲和图乙的实验装置.检查气密性良好后进行实验验证.预热后对试管进行加热(2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O)
(1)观察到图甲浓硫酸中有气泡产生,蚊香熄灭,浓硫酸的作用是干燥二氧化碳,观察图乙中的现象是蚊香燃烧更剧烈,说明有氧气产生,由资料和实验可得出的结论是湿润的二氧化碳更容易和过氧化钠反应.
(2)某化学兴趣小组对以上甲、乙装置试管中加热后的成分进行探究分析.

[提出问题]加热后的试管中残留物成分是什么呢?
[提出猜想]猜想1:只有碳酸钠 猜想2:只有碳酸氢钠 猜想3:有碳酸钠和碳酸氢钠.
[查阅资料]①碳酸钠固体受热不分解.
②碳酸氢钠溶液中滴加氯化钙溶液无明显现象,而碳酸钠溶液中滴加氯化钙溶液有白色沉淀产生.
[实验探究]
| 实验内容 | 预测现象 | 结论 |
| 实验一:取一定量残留固体于试管中,加热一段时间后,冷却,称量 | 加热前后固体质量减少(“不变”或“减少”). | 含有碳酸氢钠 |
| 实验二:取适量残留固体于试管中,加放蒸馏水充分振荡,滴入氯化钙溶液. | 溶液中产生白色沉淀 | 含有碳酸钠 |
| 结合实验一和实验二得出,猜想3正确. | ||
分析 (1)浓硫酸具有吸水性,可以用来干燥二氧化碳,氧气能够支持燃烧;
(2)根据碳酸钠和碳酸氢钠的性质以及反应的实验现象确定物质的成分;
(3)根据碳酸氢钠受热易分解解答.
解答 解•:(1)浓硫酸具有吸水性,能吸收碳酸氢钠受热分解产生的水蒸气;
观察图乙中的现象是蚊香燃烧更剧烈,说明有氧气产生,即过氧化钠和二氧化碳反应生成了氧气;
甲中和过氧化钠混合的二氧化碳是干燥的,不容易和过氧化钠反应,因此没有反应的二氧化碳能使燃烧的蚊香熄灭,而乙中的二氧化碳中含有水蒸气,容易和过氧化钠反应生成氧气,由资料和实验可得出的结论是湿润的二氧化碳更容易和过氧化钠反应;
故填:干燥二氧化碳;蚊香燃烧更剧烈;湿润的二氧化碳更容易和过氧化钠反应;
(2)碳酸氢钠可能是部分分解,故残留的固体可能是碳酸钠和碳酸氢钠的混合物,故填:有碳酸钠和碳酸氢钠;
取一定量残留固体于试管中,加热一段时间后,冷却,称量,由于含有碳酸氢钠,碳酸氢钠受热会分解生成二氧化碳和水蒸气逸出,故固体质量会减少;含有碳酸钠,则碳酸钠能与氯化钙反应生成碳酸钙白色沉淀,故猜想3正确;故填:
| 实验内容 | 预测现象 | 结论 |
| 实验一:取一定量残留固体于试管中,加热一段时间后,冷却,称量 | 加热前后固体质量 减少(“不变”或“减少”). | 含有碳酸氢钠 |
| 实验二:取适量残留固体于试管中,加放蒸馏水充分振荡,滴入 氯化钙溶液. | 溶液中 产生白色沉淀 | 含有碳酸钠 |
| 结合实验一和实验二得出,猜想 3正确. | ||
点评 本题考查的是碳酸氢钠和碳酸钠性质的实验探究,完成此题,可以依据已有的物质的性质结合物质间反应的实验现象进行.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.氧化物R2O3中氧元素的质量分数为30%,则R的相对原子质量是( )
| A. | 27 | B. | 32 | C. | 56 | D. | 112 |
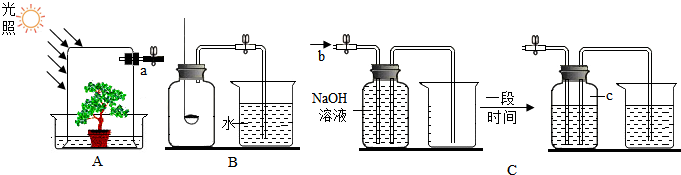
16.某课外小组的同学将玻璃罩内充满纯净的二氧化碳气体,如图A所示,在光照充足的条件下,经过一段时间后,该小组同学用注射器从a处抽取气体,测定玻璃罩内气体的成分及其含量.
【查阅资料】
①植物通过光合作用吸收二氧化碳气体,放出氧气.
②氢氧化钠和氢氧化钙性质相似,其水溶液都能与二氧化碳发生反应,
且没有气体物质生成.
【实验一】检验玻璃罩内是否含有二氧化碳气体?
【实验二】采用两种方法测定玻璃罩内气体中氧气的含量.
方法1:用如图B所示的装置测量气体中氧气的含量.
(1)实验前对该装置的气密性进行检查,小明设计了一种方法,请你帮他完成:打开止水夹,把导管末端浸没在水中,若导管内水柱下降,则装置气密性良好;
(2)将抽取出的气体用排水法收集到150ml的集气瓶中,关闭止水夹,点燃红磷;
(3)待装置冷却到室温后,打开止水夹,烧杯中的液体进入集气瓶中,体积约为100ml.
方法2:用如图C所示的装置测量气体中氧气的含量.
(1)抽取150ml的气体,缓缓地从b处通入装置中;
(2)实验结束后,c处气体的化学式为O2,集气瓶中排出液体的体积约为75ml,该方法所测得氧气约占气体总体积的50%.
【实验反思】通过对比,该小组同学发现,两种方法所得实验结果差距较大,其中实验结果更准确的是方法2.
【查阅资料】
①植物通过光合作用吸收二氧化碳气体,放出氧气.
②氢氧化钠和氢氧化钙性质相似,其水溶液都能与二氧化碳发生反应,
且没有气体物质生成.
【实验一】检验玻璃罩内是否含有二氧化碳气体?
| 实验步骤 | 实验现象 | 实验结论 |
| 抽取适量气体,注入石灰水中 | 澄清石灰水变浑浊 | 玻璃罩内含有二氧化碳. |
| 发生的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O | ||
方法1:用如图B所示的装置测量气体中氧气的含量.
(1)实验前对该装置的气密性进行检查,小明设计了一种方法,请你帮他完成:打开止水夹,把导管末端浸没在水中,若导管内水柱下降,则装置气密性良好;
(2)将抽取出的气体用排水法收集到150ml的集气瓶中,关闭止水夹,点燃红磷;
(3)待装置冷却到室温后,打开止水夹,烧杯中的液体进入集气瓶中,体积约为100ml.
方法2:用如图C所示的装置测量气体中氧气的含量.
(1)抽取150ml的气体,缓缓地从b处通入装置中;
(2)实验结束后,c处气体的化学式为O2,集气瓶中排出液体的体积约为75ml,该方法所测得氧气约占气体总体积的50%.

【实验反思】通过对比,该小组同学发现,两种方法所得实验结果差距较大,其中实验结果更准确的是方法2.
20.下列变化与性质的描述中,前者一定是物理变化,后者一定为化学性质的是(( )
| A. | 冰雪融化、光合作用 | B. | 发光放热、食物易腐败 | ||
| C. | 电解水、氢气有可燃性 | D. | 汽油挥发、钢铁易生诱 |
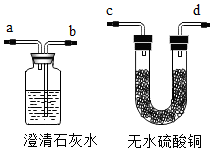
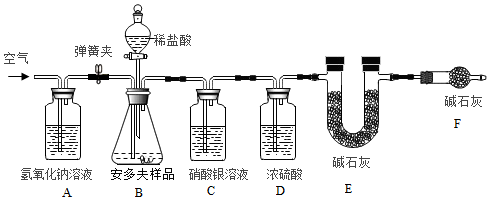
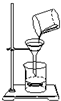 请指出如图过滤装置中的两处明显错误:
请指出如图过滤装置中的两处明显错误: