题目内容
10.2015年10月5日,中国药学家屠呦呦因发现青蒿素治疗疟疾的新疗法获诺贝尔生理学或医学奖,青蒿素的化学式为C15H22O5,下列说法正确的是( )| A. | 青蒿素是由15个碳原子、22个氢原子和5个氧原子构成 | |
| B. | 青蒿素中氧元素的质量分数最大 | |
| C. | 青蒿素属于氧化物 | |
| D. | 青蒿素中碳、氢、氧元素的质量比为90:11:40 |
分析 A、根据青蒿素的微观构成进行分析判断.
B、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
C、氧化物是只含有两种元素且其中一种元素是氧元素的化合物.
D、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
解答 解:A、青蒿素是由青蒿素分子构成的,1个青蒿素分子是由15个碳原子、22个氢原子和5个氧原子构成,故选项说法错误.
B、青篙素中碳、氢、氧三种元素的质量比为(12×15):(1×22):(16×5)=90:11:40,则青蒿素中碳元素的质量分数最大,故选项说法错误.
C、青蒿素是由碳、氢、氧三种元素的化合物,不属于氧化物,故选项说法错误.
D、青篙素中碳、氢、氧三种元素的质量比为(12×15):(1×22):(16×5)=90:11:40,故选项说法正确.
故选:D.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算等进行分析问题、解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.下列是几位同学在进行“空气与人呼出的气体成分的差异研究”的做法或想法,其中正确的是( )
| A. | 将带火星的木条分别插入空气样品和呼出气体样品中,观察现象可得出呼出气体比空气中氧气含量少的结论 | |
| B. | 将澄清石灰水分别滴入空气样品和呼出气体样品中,观察现象可得出呼出气体比空气中二氧化碳含量多的结论 | |
| C. | 取两块干燥的玻璃片,对着其中一块哈气,对比观察两块玻璃片的现象可得出呼出气体比空气中水蒸气含量多的结论 | |
| D. | 呼出的气体中除了氧气、二氧化碳、水蒸气外还有氮气等其他气体 |
9.(1)阅读下面短文并回答问题:
镁条是银白色固体,具有可燃性,在空气中点燃镁条,发出耀眼的白光,放出热量,生成一种白色的氧化镁粉末,镁的密度为1.7g/cm3,熔点为648.8℃,镁能与稀盐酸反应生成氢气.
上述叙述中:属于镁的物理性质有:银白色固体,密度为1.7g/cm3,熔点为648.8℃;
属于镁的化学性质有:具有可燃性,能与稀盐酸反应生成氢气;
可判断镁条燃烧发生化学变化的现象有:生成一种白色的氧化镁粉末.
(2)1991年,我国著名化学家张青莲教授与另一位科学家合作,测定了铟(In)元素的相对原子质量新值.铟元素的核电荷数为49,相对原子质量为115.铟原子的核外电子数为49,核内质子数为49,核内中子数为66
(3)如表是元素周期表的一部分,请根据表中信息回答下列问題:
(1)氯元素的相对原子质量是35.45,在化学反应中容易得到(填“得到”或“失去”)电子.
(2)由原子序数为8和13的元素形成的化合物的化学式是Al2O3.
(3)第二、三周期的元素排列从左至右所遵循的规律是最外层电子数由1个依次增加到8个(写一种).
镁条是银白色固体,具有可燃性,在空气中点燃镁条,发出耀眼的白光,放出热量,生成一种白色的氧化镁粉末,镁的密度为1.7g/cm3,熔点为648.8℃,镁能与稀盐酸反应生成氢气.
上述叙述中:属于镁的物理性质有:银白色固体,密度为1.7g/cm3,熔点为648.8℃;
属于镁的化学性质有:具有可燃性,能与稀盐酸反应生成氢气;
可判断镁条燃烧发生化学变化的现象有:生成一种白色的氧化镁粉末.
(2)1991年,我国著名化学家张青莲教授与另一位科学家合作,测定了铟(In)元素的相对原子质量新值.铟元素的核电荷数为49,相对原子质量为115.铟原子的核外电子数为49,核内质子数为49,核内中子数为66
(3)如表是元素周期表的一部分,请根据表中信息回答下列问題:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | 1 H 氢 1.008 | 2 He 氦 4.003 | ||||||
| 二 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 20.18 |
| 三 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(2)由原子序数为8和13的元素形成的化合物的化学式是Al2O3.
(3)第二、三周期的元素排列从左至右所遵循的规律是最外层电子数由1个依次增加到8个(写一种).
 某实验小组利用如图所示装置测量空气中氧气体积分数并取得成功.
某实验小组利用如图所示装置测量空气中氧气体积分数并取得成功. 为测定某石灰石样品中碳酸钙的含量,取该石灰石样品10g放入烧杯中,加入一定溶质质量分数的稀盐酸使之充分反应,所加稀盐酸质量与生成的二氧化碳质量关系如图所示.求:
为测定某石灰石样品中碳酸钙的含量,取该石灰石样品10g放入烧杯中,加入一定溶质质量分数的稀盐酸使之充分反应,所加稀盐酸质量与生成的二氧化碳质量关系如图所示.求: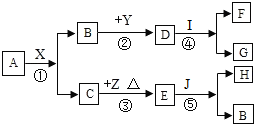 如图是中学常见的物质的转换关系图.其中A,B常温下都为无色液体,且组成元素相同,A,B,X,Y,E都为氧化物,X,E都为黑色固体,Y可用作干燥剂,F是大理石的主要成分,请回答:
如图是中学常见的物质的转换关系图.其中A,B常温下都为无色液体,且组成元素相同,A,B,X,Y,E都为氧化物,X,E都为黑色固体,Y可用作干燥剂,F是大理石的主要成分,请回答: