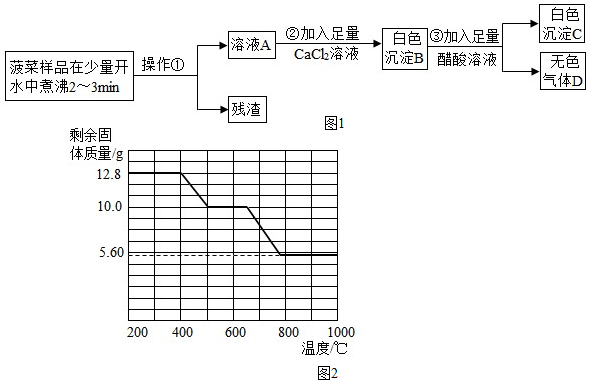
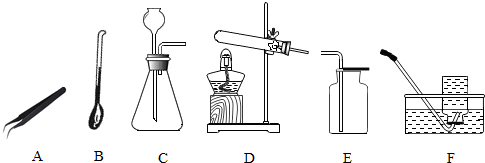
题目内容
19.某同学用氢气还原灼热氧化铜的方法测定水的组成(装置如图所示)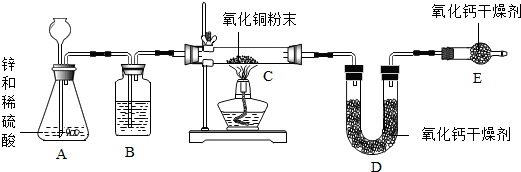
(1)B装置中盛放的液体是浓硫酸,其作用是吸收氢气中的水分.
(3)E装置的作用是防止空气中的水进入D装置,如果不连接E装置,得出的实验结论中氢氧元素的质量比大于(填大于、小于或等于)理论值.
分析 运用氢气还原氧化铜生成水和铜,要用氢气还原氧化铜测定水的组成,则氢气必须是干燥的,C装置减轻的质量就是生成的水中氧元素的质量,U形管增重即生成的水的质量.水的质量减去氧元素质量就是氢元素质量.
解答 解:运用氢气还原氧化铜生成水和铜没定水的组成,氢气须是干燥的,需用浓硫酸除去氢气中混有的水蒸气;C装置减轻的质量就是CuO中的O失去的质量,是氢气夺走了CuO中的O生成了水,U形管增重的质量就是该反应生成的水的质量,则水中H元素的质量就是水的质量减去O元素的质量,若不连接E装置,外界中的水进入D装置,使D装置增重的质量增大,氧元素质量不变,则会使氢元素质量增大,氢氧元素质量比增大.
故答案为:(1)浓硫酸;吸收氢气中的水分.
(2)防止空气中的水进入D装置;大于.
点评 典型的实验探究题,熟练掌握氢气还原氧化铜的性质和实验才能准确解答该题,要分析清楚每步实验的目的即可准确解答该题.

练习册系列答案
相关题目
10.下列实验不能达到目的是( )
| A. | 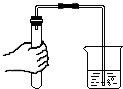 检查气密性 | B. | 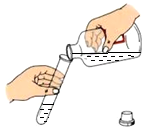 倾倒液体 | ||
| C. | 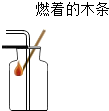 CO2的验满 | D. | 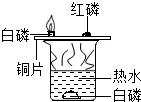 验证可燃物燃烧的条件 |
14.下列实验操作中,正确的是( )
| A. |  称量固体 | B. |  加热液体 | C. | 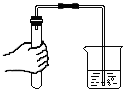 检查气密性 | D. |  倾倒液体 |
4.如图表示两种气体发生化学反应,其中相同的球代表同种原子.根据图示信息,下列说法正确的是( )
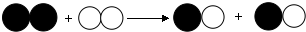

| A. | 该反应生成两种物质 | B. | 化学反应前后原子的种类不变 | ||
| C. | 该反应是复分解反应 | D. | 分子在化学变化中是不可分的 |
9.空气中体积约占$\frac{1}{5}$的气体是( )
| A. | 水蒸气 | B. | 氮气 | C. | 二氧化碳 | D. | 氧气 |