题目内容
15.向16g黄铜(由锌、铜形成的合金)样品中加入148.4g稀硫酸恰好完全反应,生成氢气质量为0.4g,则所得溶液中溶质的质量分数可能为( )| A. | 8% | B. | 10% | C. | 19.6% | D. | 20% |
分析 利用锌与硫酸反应的化学方程式,根据氢气的质量求出锌的质量以及生成硫酸锌的质量,进而求出样品中锌的质量分数以及反应后生成硫酸锌所得溶液中溶质的质量分数即可.
解答 解:设合金中锌的质量为x,硫酸锌的质量为y.
Zn+H2SO4═ZnSO4+H2↑
65 161 2
x y 0.4g
$\frac{65}{x}=\frac{161}{y}=\frac{2}{0.4g}$
x=13g,y=32.2g
反应后生成硫酸锌所得溶液中溶质的质量分数=$\frac{32.2g}{13+148.8g-0.4g}$×100%=20%
故选:D.
点评 有关反应后所得溶液的计算是初中化学的一个重点,计算溶液质量的方法一般是:所加入的所有物质的质量总和-生成沉淀的质量-生成气体的质量.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.下列有关氧原子说法不正确的是( )
| A. | 氧原子的质子数是8 | B. | 氧原子的核外电子数是8 | ||
| C. | 氧原子的相对原子质量是8 | D. | 氧是非金属元素 |
3.如图所示四个图象中,能正确表示对应变化关系的是( )
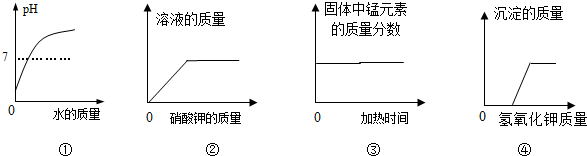

| A. | ①向一定量稀盐酸中加水稀释 | |
| B. | ②一定温度下,向水中加入硝酸钾晶体 | |
| C. | ③加热一定量的高锰酸钾固体 | |
| D. | ④向盐酸和氯化镁的混合溶液中滴加氢氧化钾溶液 |