题目内容
12.在实际生产中,研究物质的溶解度有很重要的意义.如表是某些物质在不同温度下的溶解度,请根据表中数据回答下列问题.| 温度/℃ | 0 | 20 | 40 | 60 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | |
(2)40℃时,将质量均为40g 的NaCl和KNO3分别放入盛有100g水的烧杯中,充分搅拌.下列有关所得溶液的说法正确的是bd(填字母序号).
a.得到的KNO3溶液是饱和溶液
b.两种溶液溶质的质量分数KNO3大于NaCl
c.将两种溶液均升温至60℃时,此时两种溶液均达到饱和状态
d.将两种溶液均降温至20℃时,烧杯中剩余固体的质量KNO3大于NaCl.
分析 (1)根据氯化钠的溶解度受温度的影响变化不大进行解答;
(2)根据NaCl和KNO3的溶解度以及受温度的影响情况来分析.
解答 解:(1)氯化钠的溶解度受温度的影响变化不大,所以从海水中获取粗盐采取的方法是蒸发溶剂;
(2)40℃时,氯化钠的溶解度为36.6g,那么在该温度下的100g水中,最多能溶解36.6g氯化钠就达到饱和状态;40℃时,硝酸钾的溶解度为63.9g,那么在该温度下的100g水中,最多溶解63.9g硝酸钾达到饱和状态.
若40℃时,将质量均为40g 的NaCl和KNO3分别放入盛有100g水的烧杯中,充分搅拌,
a.氯化钠溶液是饱和的,硝酸钾溶液是不饱和的,故a错误;
b.在40℃时,因为在100g水中,溶解的硝酸钾的是40g,溶解的氯化钠是36.6g,所以两溶液溶质的质量分数KNO3大于NaCl,故b正确;
c.在60℃时,氯化钠的溶解度为37.3g,60℃时,硝酸钾的溶解度为110g,将两种溶液均升温至60℃时,此时氯化钠溶液达到饱和状态,硝酸钾溶液为不饱和状态,故d错误;
d.由于在20℃时,氯化钠的溶解度是36.0g,硝酸钾的溶解度是31.6g,将两种溶液均降温至20℃时,烧杯中剩余固体的质量KNO3大于NaCl,故d正确.
故答为:(1)蒸发溶剂;(2)bd.
点评 本题难度不大,主要考查了根据固体的溶解度与温度的关系解决相关的问题,从而培养学生对知识的理解和应用.

练习册系列答案
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
2.下列有关钢铁的叙述不正确的是( )
| A. | 生铁和钢都属于铁合金 | |
| B. | 钢的硬度大于纯铁的硬度 | |
| C. | 铁丝在氧气中剧烈燃烧,火焰明亮,生成黑色固体 | |
| D. | 炼铁的主要原料有铁矿石、焦炭、石灰石 |
3.下列物质属于氧化物的是( )
| A. | CaSO4 | B. | Al2O3 | C. | K2CO3 | D. | NaNO3 |
20.下列实验操作中,正确的是( )
| A. | 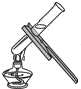 给液体加热 | B. | 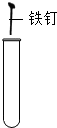 放入铁钉 | C. | 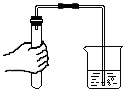 检查气密性 | D. | 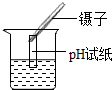 测溶液的酸碱度 |
2. 要使右图装置中的小气球鼓起来,则使用的固体和液体可以是 ①硝酸铵和水; ②铁和稀硫酸;③固体氢氧化钠和水; ④食盐和水; ⑤石灰石和稀盐酸; ⑥二氧化锰和双氧水.其中正确的是( )
要使右图装置中的小气球鼓起来,则使用的固体和液体可以是 ①硝酸铵和水; ②铁和稀硫酸;③固体氢氧化钠和水; ④食盐和水; ⑤石灰石和稀盐酸; ⑥二氧化锰和双氧水.其中正确的是( )
 要使右图装置中的小气球鼓起来,则使用的固体和液体可以是 ①硝酸铵和水; ②铁和稀硫酸;③固体氢氧化钠和水; ④食盐和水; ⑤石灰石和稀盐酸; ⑥二氧化锰和双氧水.其中正确的是( )
要使右图装置中的小气球鼓起来,则使用的固体和液体可以是 ①硝酸铵和水; ②铁和稀硫酸;③固体氢氧化钠和水; ④食盐和水; ⑤石灰石和稀盐酸; ⑥二氧化锰和双氧水.其中正确的是( )| A. | ①②③④⑥ | B. | ②④⑤⑥ | C. | ②③⑤⑥ | D. | ①②④⑤⑥ |
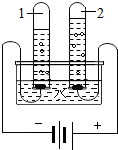 水是重要的自然资源.
水是重要的自然资源.