题目内容
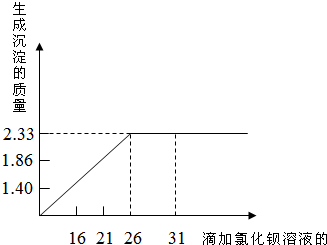
 某校课外活动小组同学在测定由氯化钠和硫酸钠形成混合物的组成时,进行了以下实验:取20g混合物全部溶于水,将得到的溶液等分为4份,然后分别加入一定量未知质量分数的氯化钡溶液,生成沉淀的质量与滴加氯化钡溶液的关系如坐标所示.
某校课外活动小组同学在测定由氯化钠和硫酸钠形成混合物的组成时,进行了以下实验:取20g混合物全部溶于水,将得到的溶液等分为4份,然后分别加入一定量未知质量分数的氯化钡溶液,生成沉淀的质量与滴加氯化钡溶液的关系如坐标所示.请计算:
(1)未知氯化钡溶液中溶质的质量分数.
(2)原混合物中硫酸钠的质量分数是多少.
分析:氯化钠和硫酸钠的混合物中硫酸钠与氯化钡反应生成硫酸钡沉淀和氯化钠,而混合物中的氯化钠不能与氯化钡反应;因此由生成沉淀硫酸钡的质量可计算出混合物中硫酸钠的质量和反应氯化钡的质量;从而求出氯化钡溶液的溶质质量分数及混合物中硫酸钠的质量分数;
解答:解:(1)由图象可以看出,当滴加氯化钡溶液的质量为2g时,5g混合物溶液中的硫酸钠全部完全反应,生成硫酸钡沉淀2.3g
设氯化钡质量为y
Na2SO4+BaCl2═2NaCl+BaSO4↓
208 233
y 2.33g
=
y=2.08g
氯化钡溶液的溶质质量分数为
×100%=8%
(2)20g混合物溶于水,将得到的溶液分成4份,每份溶液中混合物5g
设每份溶液中硫酸钠的质量为x
Na2SO4+BaCl2═2NaCl+BaSO4↓
142 233
x 2.33g
=
x=1.42g
混合物中硫酸钠的质量分数
=×100%=28.4%
答:(1)氯化钡溶液中溶质质量分数为8%
(2)混合物中硫酸钠的质量分数为28.4%;
设氯化钡质量为y
Na2SO4+BaCl2═2NaCl+BaSO4↓
208 233
y 2.33g
| 208 |
| 233 |
| y |
| 2.33g |
y=2.08g
氯化钡溶液的溶质质量分数为
| 2.08g |
| 26g |
(2)20g混合物溶于水,将得到的溶液分成4份,每份溶液中混合物5g
设每份溶液中硫酸钠的质量为x
Na2SO4+BaCl2═2NaCl+BaSO4↓
142 233
x 2.33g
| 142 |
| 233 |
| x |
| 2.33g |
x=1.42g
混合物中硫酸钠的质量分数
| 1.42g |
| 5g |
答:(1)氯化钡溶液中溶质质量分数为8%
(2)混合物中硫酸钠的质量分数为28.4%;
点评:根据图象可以看出,硫酸钡与氯化钡完全反应时生成硫酸钡沉淀的质量,这是解此题的关键.

练习册系列答案
相关题目
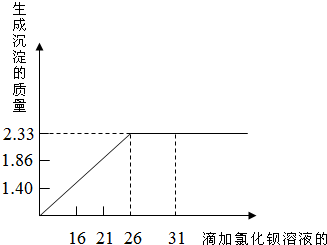 某校课外活动小组同学在测定由氯化钠和硫酸钠形成混合物的组成时,进行了以下实验:取20g混合物全部溶于水,将得到的溶液等分为4份,然后分别加入一定量未知质量分数的氯化钡溶液,生成沉淀的质量与滴加氯化钡溶液的关系如坐标所示.
某校课外活动小组同学在测定由氯化钠和硫酸钠形成混合物的组成时,进行了以下实验:取20g混合物全部溶于水,将得到的溶液等分为4份,然后分别加入一定量未知质量分数的氯化钡溶液,生成沉淀的质量与滴加氯化钡溶液的关系如坐标所示.