题目内容
5.科学施肥是实现农业增产的重要手段.硫酸铵[(NH4)2SO4]、硝酸铵(NH4NO3)、尿素[CO(NH2)2]是常用的氮肥,对提高农作物产量有重要作用.(1)上述三种物质中属于有机物的是尿素.
(2)硝酸铵(NH4NO3)中氮元素、氢元素、氧元素的质量最简整数比为7:1:12.
(3)为测定某种硫酸铵[(NH4)2SO4]化肥样品中氮元素的质量分数,甲、乙两位同学分别按自己设计的方案进行了实验(样品中杂质不含有氮元素、可溶,且不参与反应).
甲同学的方案:称取13.6g样品溶入足量水中,再向其中加入足量的氯化钡溶液,充分反应后将沉淀过滤、洗涤、干燥,得到白色固体23.3g.
乙同学的方案:称取13.6g样品,与足量的浓氢氧化钠溶液混合加热,充分反应后,将获得的气体直接用足量的浓硫酸吸收,浓硫酸增重3.9g.
请回答下列问题:
①上述不合理的方案是方案乙同学的方案(选填“甲”或“乙”),简述理由浓硫酸会吸收水蒸气和氨气.
②选用合理方案来计算该硫酸铵[(NH4)2SO4]化肥样品中氮元素的质量分数.(写出计算步骤,计算结果保留到0.1%)
分析 (1)根据有机物是指含有碳元素的化合物解答;
(2)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行解答硝酸铵NH4NO3中氮元素、氢元素、氧元素的质量比;
(3)根据浓硫酸既会吸收水分,也会吸收碱性气体进行分析;
根据氯化钡和硫酸铵反应生成硫酸钡沉淀和氯化铵,然后结合白色沉淀的质量计算氮元素的质量进行解答.
解答 解:
(1)(NH4)2SO4、NH4NO3、CO(NH2)2是常见的化肥,(NH4)2SO4、NH4NO3是铵盐属于无机物,尿素是含有碳元素的化合物,属于有机物;
(2)化合物中各元素质量比=各元素的相对原子质量×原子个数之比,因此硝酸铵(NH4NO3)中氮、氢、氧的质量比为:(14×2):(4×1):(16×3)=7:1:12;
(3)①(NH4)2SO4与NaOH溶液反应生成氨气,同时有挥发的水蒸气,所以浓硫酸吸收的气体为水蒸气和氨气,所以不能确定氨气的质量,故方案乙不合理;
故答案为:方案乙;浓硫酸会吸收水蒸气和氨气;
②设硫酸铵中含有氮元素质量为x,
通过(NH4)SO4+BaCl2=BaSO4↓+2NH4Cl可知
2N-------(NH4)SO4-----BaSO4
28 233
x 23.3g
$\frac{28}{x}=\frac{233}{23.3g}$
x=2.8g
所以该(NH4)2SO4化肥样品中氮元素的质量分数为:$\frac{2.8g}{13.6g}$×100%=20.6%.
答案:
(1)尿素;
(2)7:1:12;
(3)
①方案乙;浓硫酸会吸收水蒸气和氨气;
②(NH4)2SO4化肥样品中氮元素的质量分数20.6%.
点评 本题主要考查学生对物质中某元素的质量分数以及各元素质量比的计算,难度不大,但要注意计算的格式和结果的准确性.

 阅读快车系列答案
阅读快车系列答案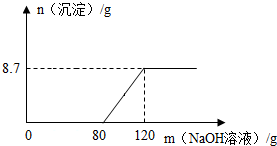 做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中的溶质成分产生了兴趣,请你于他们一起进行以下探究.
做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中的溶质成分产生了兴趣,请你于他们一起进行以下探究.【提出问题】溶液中的溶质是什么物质?
【作出猜想】
(1)甲同学认为溶液中的溶质只有Na2SO4一种物质.
(2)乙同学认为溶液中的溶质有Na2SO4和H2SO4两种物质.
(3)丙同学认为溶液中的溶质有Na2SO4和NaOH两种物质.
(4)丁同学认为溶液中的溶质有Na2SO4、NaOH和H2SO4三种物质.
通过进一步讨论,大家一致认为以上丁(填甲、乙、丙、丁)同学的猜想肯定错,无需实验验证.
【查阅资料】
①Na2SO4溶液显中性.
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)和另外一种物质.
【实验验证】
| 实验操作 | 实验现象 | 实验结论 | |
| 乙同学 实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管内的溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 猜想(2)成立 |
| 丙同学 实验 | 取中和反应后的溶液少许于试管中,向试管内滴加几滴无色酚酞试液 | 无色溶液变成红色 | 猜想(3)成立 |
【知识拓展】
(1)生活中能否用铝制品来盛放强碱性溶液?不能(选填“能”或“不能”)
(2)乙同学的实验中铝片与H2SO4溶液发生了反应,请写出铝与该溶液发生反应的化学方程式
2Al+3H2SO4═Al2(SO4)3+3H2↑.
(3)镁和铝在元素周期表中处于相邻位置,向盛有100g稀硫酸的烧杯中加入一定量的Mg粉,固体完全溶解后,再向所得溶液中加入NaOH溶液,所得沉淀质量与加入NaOH溶液的质量关系如图所示.
①计算该NaOH溶液溶质的质量分数.(要求写出计算过程)
②计算该100g稀硫酸中所含溶质硫酸的质量.(要求写出计算过程)
| A. | 排水法收集氧气时,当导管口开始有气泡冒出时立即收集 | |
| B. | 稀释浓硫酸时,将浓硫酸沿烧杯壁缓缓注入盛有水的饶杯中,并用玻璃棒不断搅拌 | |
| C. | 过滤时,用玻璃棒在过滤器中不断搅拌 | |
| D. | 氢气、甲烷等可燃性气体点燃前进行验纯 |
| A. | 在含砂粒较多、潮湿、透气的土壤中 | B. | 在干燥、致密、透气的土壤中 | ||
| C. | 在潮湿、疏松、透气的土壤中 | D. | 在呈酸性的潮湿土壤中 |
 经过一年的学习,我们对“酸碱盐”有了一定的认识,请回答下列有关问题.
经过一年的学习,我们对“酸碱盐”有了一定的认识,请回答下列有关问题.(1)下列说法中不正确的是B.
A、酸和碱中一定都含有氢元素
B、氯化钠由氯化钠离子构成
C、多数酸和碱都有腐蚀性
D、浓硫酸可用作某些气体的干燥剂
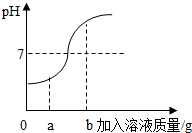
(2)在用稀盐酸和氢氧化钠溶液进行中和反应的实验时,反应过程中溶液的酸碱度变化如图所示,该图横坐标代表的是NaOH溶液的质量.当加入该溶液的质量为ag时,所得溶液中含量最多的溶质为(写化学式)NaCl.
(3)某敞口放置的氢氧化钠溶液已经变质,请用化学方程式表示其变质的原因.
(4)为了证明该瓶氢氧化钠溶液未完全变质,进行了以下实验,请将如表填写完整.
| 实验操作 | 现象 | 结论或化学方程式 |
| 取少量该样品,滴加足量的BaCl2溶液,过滤 | 有白色沉淀生成 | 方程式为:Na2CO3+BaCl2=BaCO3↓+2NaCl |
| 在滤液中滴加酚酞溶液 | 滤液显红色 | 样品未完全变质 |
| A. | 钾肥 | B. | 磷肥 | C. | 氮肥 | D. | 复合肥 |
 ”表示氧原子,“
”表示氧原子,“ ”表示氢原子)请回答下列问题:
”表示氢原子)请回答下列问题:
 如图所示是冶铁的反应原理,写出一氧化碳与氧化铁反应的现象固体由红棕色变化为黑色,反应方程式是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,图中右边酒精的作用是点燃没有参与反应的CO.
如图所示是冶铁的反应原理,写出一氧化碳与氧化铁反应的现象固体由红棕色变化为黑色,反应方程式是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,图中右边酒精的作用是点燃没有参与反应的CO. 化学与生活密切相关.请根据所学知识回答下列问题:
化学与生活密切相关.请根据所学知识回答下列问题: