题目内容
7.现有氯酸钾和二氧化锰的混合物共33g,待反应不再有气体生成后,将试管冷却,得到氧气9.6g,求:(1)剩余固体的质量为多少克?
(2)剩余固体中含有的各物质为多少克?
分析 氯酸钾在二氧化锰催化作用下受热分解生成氯化钾和氧气,根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:(1)因反应中氧气为气体,则剩余固体质量为33g-9.6 g═23.4g,
(2)因反应至不再有气体生成,则氯酸钾完全分解,
剩余固体中含氯化钾和二氧化锰,设氯化钾的质量为x,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,
149 96
x 9.6g
$\frac{149}{x}$=$\frac{96}{9.6g}$,
x=14.9g,
即氯化钾的质量为14.9g,
则二氧化锰质量为23.4g-14.9g═8.5g,
答:剩余固体的质量为23.4g,其中氯化钾质量为14.9 g,二氧化锰质量质量为8.5g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
17.某中学研究性学习小组的同学为了测定黄铜(铜锌合金)中锌的质量分数,取4份不同质量的黄铜样品,分别加入50克稀硫酸,结果如表:
(1)哪几次反应中硫酸有剩余1、2.
(2)上表中M的数值0.5.
(3)计算黄铜中锌的质量分数.
(4)计算稀硫酸的质量分数.
| 实验序号 | 1 | 2 | 3 | 4 |
| 加入样品的质量/克 | 10 | 20 | 30 | 40 |
| 稀硫酸的质量/克 | 50 | 50 | 50 | 50 |
| 生成H2的质量/克 | 0.2 | 0.4 | 0.5 | M |
(2)上表中M的数值0.5.
(3)计算黄铜中锌的质量分数.
(4)计算稀硫酸的质量分数.
18.在一密闭容器内加入a、b、c、d四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如图,下列说法中正确的是( )
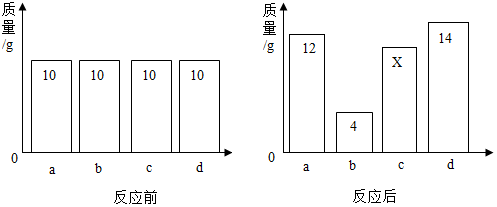

| A. | 该反应为化合反应 | |
| B. | 丙一定为该反应的催化剂 | |
| C. | 次反应中b物质和d物质的质量比为3:2 | |
| D. | d的相对分子质量是a的2倍 |
15.已知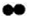 、
、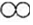 、
、 分别表示X、Y、Z三种不同的气体分子,其在一定条件下的变化如图所示,由图示获得的下列信息中正确的是( )
分别表示X、Y、Z三种不同的气体分子,其在一定条件下的变化如图所示,由图示获得的下列信息中正确的是( )
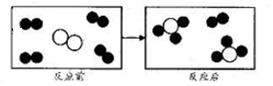
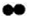 、
、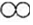 、
、 分别表示X、Y、Z三种不同的气体分子,其在一定条件下的变化如图所示,由图示获得的下列信息中正确的是( )
分别表示X、Y、Z三种不同的气体分子,其在一定条件下的变化如图所示,由图示获得的下列信息中正确的是( )
| A. | 反应前后分子的种类发生变化 | B. | Z一定是氧化物 | ||
| C. | 该反应可表示为4X+Y=2Z | D. | 反应物和生成物都有单质 |
3.我国纪念2017年“世界水日”和“中国水周”活动的宣传主题为“落实绿色发展理念,全面推行河长制”.下列做法不符合这一主题的是( )
| A. | 推广使用无磷洗衣粉,有利于保护水资源 | |
| B. | 可通过过滤的方法除去受污染水中的有毒可溶性苯 | |
| C. | 加强工业废水的排放监控,坚持经处理后达标排放 | |
| D. | 合理施用农药、化肥,以减少水体污染 |
