题目内容
18.如图是实验室常用的装置,请回答有关问题:
(1)写出图中标号仪器的名称:①试管,②锥形瓶.
(2)实验室用装置A与C连接制取并收集O2,则装置A中反应的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,实验完毕后,应先将导管移出水面,然后再熄灭酒精灯.
(3)在用H2O2和MnO2制取O2 的反应中,MnO2的作用是催化作用,若用此反应制取O2并收集较纯净的应选择装置的连接顺序是BC(填装置序号).
(4)实验室制取CO2反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,可选用的发生装置是B;选用的收集装置是D(填装置序号)理由是二氧化碳的密度比空气的密度大;证明集满CO2的方法将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了.
(5)如图F所示,向烧杯中倾倒二氧化碳,现象是:下面的蜡烛先熄灭,上面的蜡烛后熄灭,说明二氧化碳具有的性质是既不能燃烧也不能支持燃烧且密度比空气的密度大,因此,二氧化碳可用于灭火.
(6)都可用于制取O2、CO2和H2的发生装置是B(填装置序号).
分析 试管、锥形瓶是常用的反应容器,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净.实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了.如图F所示,向烧杯中倾倒二氧化碳,现象是:下面的蜡烛先熄灭,上面的蜡烛后熄灭,说明二氧化碳具有的性质是既不能燃烧也不能支持燃烧,且密度比空气的密度大,证明集满CO2的方法:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集.
解答 解:(1)试管、锥形瓶是常用的反应容器,故答案为:试管;锥形瓶;
(2)如果用氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂;故答案为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;导管;熄灭酒精灯;
(3)如果用双氧水和二氧化锰制氧气就不需要加热,其中二氧化锰起催化作用;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净;故答案为:催化作用;BC;
(4)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;B;D;二氧化碳的密度比空气的密度大;将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;
(5)如图F所示,向烧杯中倾倒二氧化碳,现象是:下面的蜡烛先熄灭,上面的蜡烛后熄灭,说明二氧化碳具有的性质是既不能燃烧也不能支持燃烧,且密度比空气的密度大,证明集满CO2的方法:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;故答案为:下面的蜡烛先熄灭,上面的蜡烛后熄灭;既不能燃烧也不能支持燃烧;密度大;将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;
(6)如果用双氧水和二氧化锰制氧气就不需要加热,实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;实验室是用锌粒和稀硫酸在常温下反应制氢气的,因此不需要加热;故答案为:B;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的验满方法和性质等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| A. | 金属铝比金属锌更耐腐蚀,说明锌比铝活动性强 | |
| B. | 气体受热后体积膨胀,说明受热后分子变大了 | |
| C. | 配制硫酸铜溶液不宜用铁制容器,说明铁的金属活动性比铜强 | |
| D. | 金属锌粒与稀硫酸反应适于实验室制取氢气,说明两者反应的速率特别快 |

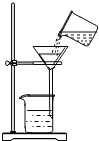 程伟同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉未搅拌溶解,静置一会儿后,采用下图所示装置进行过滤,
程伟同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉未搅拌溶解,静置一会儿后,采用下图所示装置进行过滤,