题目内容
11.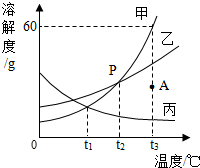 图为甲、乙、丙三种物质的溶解度曲线.
图为甲、乙、丙三种物质的溶解度曲线.(1)图中P点表示的意义t2℃时,甲、乙物质的溶解度相等.
(2)t3℃时,A点表示溶液为乙的不饱和溶液(填“饱和”或“不饱和”溶液).
(3)t3℃时,完全溶解6g甲物质至少需要10g水,该温度下的饱和溶液溶质质量分数最大为37.5%.
(4)将t3℃时质量相等的甲的饱和溶液与丙的饱和溶液均降温到t1℃,所得溶液质量大小关系为:甲<丙(填“<”、“>”或“=”).
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.将t3℃时质量相等的甲的饱和溶液与丙的饱和溶液均降温到t1℃,所得溶液质量大小关系为甲小于丙,因为丙由饱和变为不饱和溶液,甲有固体析出.
解答 解:(1)图中P点表示的意义:t2℃时,甲、乙物质的溶解度相等;故答案为:t2℃时,甲、乙物质的溶解度相等;
(2)t3℃时,A点表示溶液为乙的不饱和溶液,因为A点在乙的溶解度曲线下方,故答案为:不饱和溶液;
(3)t3℃时,甲的溶解度是60g,因此完全溶解6g甲物质至少需要10g水,该温度下的饱和溶液溶质质量分数=$\frac{60g}{160g}×100%=37.5%$,故答案为:10;37.5%;
(4)将t3℃时质量相等的甲的饱和溶液与丙的饱和溶液均降温到t1℃,所得溶液质量大小关系为甲小于丙,因为丙由饱和变为不饱和溶液,甲有固体析出,故答案为:<;
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
1.下列变化属于化学变化的是( )
| A. | 西瓜榨汁 | B. | 灯泡通电发光放热 | ||
| C. | 木已成舟 | D. | 钢铁生锈 |
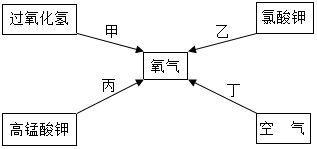
2.加热氯酸钾但不加入二氧化锰,其结果是( )
| A. | 不产生氧气 | B. | 产生氧气的速率减慢 | ||
| C. | 产生氧气的质量减少 | D. | 产生氧气的速率加快 |
16. 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )| A. | 乙一定是化合物 | |
| B. | 丙可能为该反应的催化剂 | |
| C. | 在t1-t2时间段内,四种物质的质量不再改变 | |
| D. | 该反应中,甲、乙的质量变化之比为7:2 |
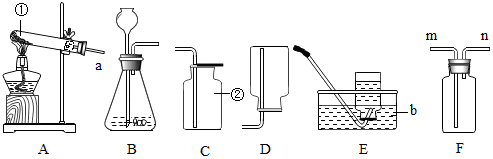
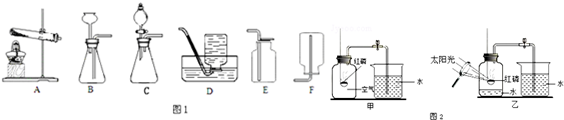
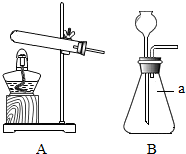
20.根据如图中的实验装置,回答问题:
(1)写出图B中仪器a的名称:锥形瓶.
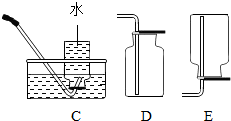
(2)实验室用加热氯酸钾和二氧化锰混合物制取氧气的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,发生和收集装置为A、C(或D)(填字母).
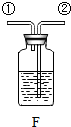
(3)实验室用石灰石和稀盐酸反应制取二氧化碳,其中常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的F装置来除去,则混合气体应从F装置的②端口(填“①”或“②”)通入,F中发生的化学方程式为NaHCO3+HCl═NaCl+H2O+CO2↑.
| 发生装置 | 收集装置 | 洗气装置 |
 |  |  |
(2)实验室用加热氯酸钾和二氧化锰混合物制取氧气的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,发生和收集装置为A、C(或D)(填字母).
(3)实验室用石灰石和稀盐酸反应制取二氧化碳,其中常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的F装置来除去,则混合气体应从F装置的②端口(填“①”或“②”)通入,F中发生的化学方程式为NaHCO3+HCl═NaCl+H2O+CO2↑.