题目内容
1.为验证质量守恒定律,某同学设计了下列如图实验: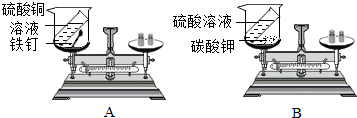
(1)请写出反应的化学方程式:A组药品混合后:Fe+CuSO4═FeSO4+Cu,B组药品混合后:K2CO3+H2SO4=K2SO4+H2O+CO2↑.
(2)A组药品混合前、后质量关系为:m前=m后,该实验正确的反映了参加反应的物质与反应生成物之间的质量关系.请从原子的角度,简要分析原因:化学反应前后原子的种类、数目和质量没有发生改变.
(3)B组药品混合前、后质量关系为:m前>m后,该实验不能正确反映了参加的物质与反应生成物之间的质量关系,请分析原因是反应生成的二氧化碳逸散到空气中,该实验若试剂不变,应如何改进此装置应在密闭的容器中进行.
分析 (1)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
实验I镁条燃烧,镁条与空气中的氧气发生化合反应生成白色固体氧化镁;反应前所称量为金属镁的质量,反应后所称量的质量为金属氧化物氧化镁的质量;
(2)反应前后质量之所以守恒,是由于化学变化是一个“分子破裂成原子,原子重新组合成分子”的过程,此过程中,原子种类、原子个数、原子的质量都不改变;
(3)质量守恒是指参加反应的物质的总质量不变,而实验B没有称量放出气体质量的质量,因此,不能说明反应前后质量不变.
解答 解:(1)A组药品混合后:铁与硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式是:Fe+CuSO4═FeSO4+Cu.
B组药品混合后:碳酸钾与硫酸反应生成硫酸钾、水和二氧化碳,反应的化学方程式为:K2CO3+H2SO4=K2SO4+H2O+CO2↑.
(2)化学变化是一个“分子破裂成原子,原子重新组合成分子”的过程,此过程中,原子种类、原子个数、原子的质量都不改变,所以,化学变化前后虽然物质发生了改变,但构成物质(分子)的原子既不减少也不改变,变化前后总质量不变;
故答案为:化学反应前后原子的种类、数目和质量没有发生改变;
(3)B实验中的硫酸和碳酸钾溶液反应产生二氧化碳是气体,会逸出容器,使剩下物质的质量减轻,因此使得天平不平衡,所以应在密闭的容器中进行;
答案:
(1)Fe+CuSO4═FeSO4+Cu.K2CO3+H2SO4=K2SO4+H2O+CO2↑.
(2)化学反应前后原子的种类、数目和质量没有发生改变;
(3)反应生成的二氧化碳逸散到空气中;应在密闭的容器中进行.
点评 验证质量守恒定律时,有气体参加的实验必须密封,若不密封因气体质量的影响而造成所得的生成物的质量与反应物的质量不相等,不能得出质量守恒的结论.

 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 某化学兴趣小组在完成酸、碱、盐的化学性质实验时,做了如下实验:向碳酸钠溶液中加入一瓶标签破损的溶液M(如图),有白色沉淀产生,过滤后得到澄清滤液,同学们对该实验进行了如下探究.
某化学兴趣小组在完成酸、碱、盐的化学性质实验时,做了如下实验:向碳酸钠溶液中加入一瓶标签破损的溶液M(如图),有白色沉淀产生,过滤后得到澄清滤液,同学们对该实验进行了如下探究.探究一:M溶液中的溶质是什么?
(1)【提出猜想】:该小组同学认为M溶液中的溶质有两种可能:猜想①是:Ba(OH)2,猜想②是BaCl2.
【收集资料】:CaCl2的水溶液呈中性.
(2)【设计实验】:同学们设计了如下方案并进行实验:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量M溶液于试管中,向其中滴入酚酞试液 | 溶液变红 | 猜想①正确 |
【提出猜想】:猜想一:NaOH和Na2CO3;
猜想二:NaOH和Ba(OH)2;
猜想三:NaOH.
(3)【实验验证】:同学们针对“猜想一”进行如下实验:
| 实验操作 | 实验现象 | 实验结论 |
| 取样于试管中,滴入几滴稀盐酸 | 没有气泡产生 | “猜想一”不成立 |
(4)【继续探究】:设计如表实验方案确定滤液中溶质的组成.
| 实验操作 | 实验现象 | 实验结论 |
| 分别取少量滤液于A、B两支试管中,A中加入CaCl2溶液,B中加入Na2CO3溶液. | 若A中产生白色沉淀,B中没有沉淀 | “猜想一”成立 |
| 若A中没有沉淀,B中产生白色沉淀 | “猜想二”成立 | |
| 若A、B中都没有沉淀产生 | “猜想三”成立 |
①为防止标签被腐蚀而破损,倾倒液体时应标签要向着手心;
②在分析反应后所得溶液中溶质时,除考虑可溶性的生成物之外,还应考虑反应的程度(合理即可).
| A. | 溶液都是无色透明的 | B. | 水可以溶解任何物质 | ||
| C. | 均一、稳定的液体都是溶液 | D. | 饱和溶液不一定是浓溶液 |
| A. | 铜能导电 | B. | 氢氧化钙微溶于水 | ||
| C. | 镁能与氧气反应 | D. | 常温下甲烷是无色无味气体 |
| A. | 人体无法消化吸收纤维素,所以食物中的纤维素对人体毫无意义 | |
| B. | 煤气中毒主要是一氧化碳与血红蛋白结合,使血红蛋白失去输氧能力 | |
| C. | 人体缺少必需的微量元素不会影响身体健康 | |
| D. | 低血糖发作时,吃馒头比喝葡萄糖水见效快 |
| A. | 将金属铜和锌制成黄铜合金 | B. | 石墨转化为金刚石 | ||
| C. | 煮沸的方法将硬水转化为软水 | D. | 植物的光合作用 |
| A. | 空气是一种化合物--含有多种分子 | |
| B. | 氢气和液氧的化学性质相同--两者的分子构成相同 | |
| C. | 盛有香水的瓶子敞口久置后香水“消失--分子在不断运动 | |
| D. | 化学反应前后物质总质量不变--反应前后分子的种类和个数都不变 |