题目内容
16.(1)某学生发现滴瓶中出现悬浮物,如图1所示进行过滤.他的操作出现了多处错误,请写出其中的两个错误:(提示:用滴瓶而未用烧杯倾倒液体不算错.)
错误1倾倒溶液时没有用玻璃棒引流
错误2漏斗下端管口没有紧贴盛放滤液的烧杯内壁
(2)通过对比得出结论,是科学探究的重要方法,对比实验是化学实验中常用的实验手段.请按要求回答下列问题:
①在学习过程中,我们做了如图3、图4所示的两个实验,请写出根据这两个实验所能得出的结论.
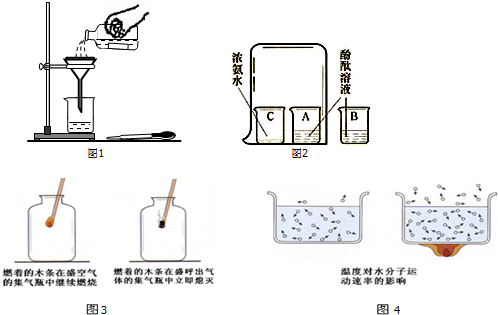
“图3”实验得出的结论空气中所含氧气比呼出气体多;
“图4”实验得出的结论温度越高,水分子(或分子)运动越快.
②通过学习我们已经知道,氨水能使酚酞溶液变红.在如图2所示的实验中,能说明氨分子在不断运动的实验现象是:A杯中酚酞溶液变红、B杯中酚酞溶液不变红(或不变色).
分析 (1)根据过滤液体时,注意“一贴、二低、三靠”的原则,观察图示的操作,指出操作中存在的错误即可;
(2)
①通过比较可知图一探究的呼出气体和空气中氧气含量的实验,而图二探究的是温度对分子运动快慢的实验.
②根据分子是不断运动的这一特点可以得出该实验的结论.
解答 解:
(1)不使用玻璃棒引流,会造成过滤时液体溅出;漏斗下端管口未紧靠烧杯内壁,会使液体溅出;滤纸不能高于漏斗边缘,否则会使滤液浑浊;倾倒液体时,标签应向着手心,图中标签没有向着手心,容易腐蚀标签;胶头滴管用完,应清洗干净,胶头在上,竖直放入烧杯中,图中胶头滴管平放在桌面上,容易腐蚀胶帽等.
(2)
①图一中将燃着的木条分别伸入盛有空气和呼出气体的集气瓶中而得出了不同的实验现象,可以看出该实验探究的是呼出气体和空气中氧气含量;图二中可以看出是在不同的温度下探究分子运动快慢的实验.
②根据氨水能使酚酞溶液变红这一原理,来比较在不同环境中的酚酞试液,来观察酚酞是否变红,通过对照可以得出分子是不断运动的结论.
答案:
(1)错误1:倾倒溶液时没有用玻璃棒引流;
错误2:漏斗下端管口没有紧贴盛放滤液的烧杯内壁.
(2)
①“图1”:空气中所含氧气比呼出气体多
“图2”:温度越高,水分子(或分子)运动越快
②A杯中酚酞溶液变红、B杯中酚酞溶液不变红(或不变色)
点评 本题难度不大,主要考查了过滤的原理、注意事项(“一贴、二低、三靠”),培养了学生分析问题、解决问题的能力.熟练掌握分子的性质,能够根据实验现象分析出实验要探究的内容,然后做出正确的结论.

练习册系列答案
相关题目
6.化学课上,同学们对人体呼出的气体中的主要成分及含量非常好奇,设计了如下实验进行相关的探究.
【提出问题】呼出的气体中有哪些主要成分?它们的含量是多少?
【查阅资料】①呼出的气体中仍含有O2;
②CO2难溶于饱和NaHCO3溶液;
③氢氧化钠能与二氧化碳反应生成可溶性的碳酸钠和水.
【假设与猜想】呼出的气体中主要成分是N2、O2、CO2、水蒸气等.
【设计方案并实验】实验I:定性检验呼出的气体中含有CO2、O2和水蒸气.
实验Ⅱ:定量测定呼出的气体中N2的含量.
同学们在老师的指导下设计了如下列图所示装置(B是带刻度的量气装置).
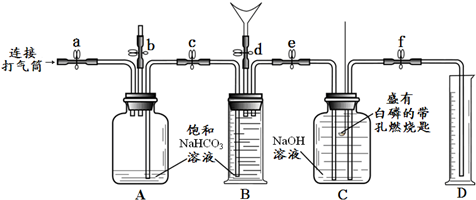
【实验反思】
(1)该实验设计依据的N2性质有ABCD(填字母序号).
A.不能与白磷发生反应 B.难溶于水
C.不能和NaOH溶液反应 D.不能燃烧,也不支持燃烧
E.无色无味的气体 F.相同条件下,密度比空气略小
(2)若上述实验所测O2的体积分数偏小,结合实验具体情况分析其可能原因是如果C装置没有完全冷却即打开止水夹f,则会由于C中温度较高气体受热膨胀,而使D中液体进入到C中减少,D中剩余液体大于400mL,则所测O2的体积分数会偏小.
【提出问题】呼出的气体中有哪些主要成分?它们的含量是多少?
【查阅资料】①呼出的气体中仍含有O2;
②CO2难溶于饱和NaHCO3溶液;
③氢氧化钠能与二氧化碳反应生成可溶性的碳酸钠和水.
【假设与猜想】呼出的气体中主要成分是N2、O2、CO2、水蒸气等.
【设计方案并实验】实验I:定性检验呼出的气体中含有CO2、O2和水蒸气.
| 实验操作 | 主要实验现象 | 实验结论 |
 | 澄清石灰水变浑浊 | 呼出的气体中含有CO2 |
 | 燃着的蜡烛逐渐熄灭(或燃着的蜡烛并不立即熄灭、蜡烛继续燃烧一段时间再熄灭等) | 呼出的气体中含有O2 |
 | 玻璃片上出现无色液滴 | 呼出的气体中含有水蒸气 |
同学们在老师的指导下设计了如下列图所示装置(B是带刻度的量气装置).

| 实验操作 | 主要实验现象 | 实验结论及解释 | |
| ① | 检查装置的气密性. 向装置中加入药品. 关闭止水夹a~f. | 装置的气密性良好. | |
| ② | 打开b、c、d,向B中吹入一定量气体后关闭d,并冷却到室温. | B中液体进入到A中,B中液体减少500mL. | 收集500mL气体. |
| ③ | 关闭b,打开a、e、f,用打气筒向A中缓缓充气,直到B中气体刚好全部排出. | A中液面下降,B中液面上升至最高,C中左侧导管口有气泡产生,且C中液面下降,液体沿导管流入D中,D中液体为475mL. | 反应的化学方程式为CO2+2NaOH═Na2CO3+H2O. |
| ④ | 关闭e、f,用凸透镜聚光引燃白磷. | 白磷燃烧,产生大量白烟,放出大量热. | 反应的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5. |
| ⑤ | 待白磷熄灭并冷却到室温,打开f. | D中的液体部分进入C中,D中剩余液体为400mL. | 呼出的气体中含有N2,且氮气的体积分数为80%. |
(1)该实验设计依据的N2性质有ABCD(填字母序号).
A.不能与白磷发生反应 B.难溶于水
C.不能和NaOH溶液反应 D.不能燃烧,也不支持燃烧
E.无色无味的气体 F.相同条件下,密度比空气略小
(2)若上述实验所测O2的体积分数偏小,结合实验具体情况分析其可能原因是如果C装置没有完全冷却即打开止水夹f,则会由于C中温度较高气体受热膨胀,而使D中液体进入到C中减少,D中剩余液体大于400mL,则所测O2的体积分数会偏小.
7.如图为某反应的微观示意图,不同的球代表不同元素的原子.下列说法中正确的是( )

| A. | A、B、C分别代表3种不同的物质 | |
| B. | 该反应原子种类在反应前后没有改变是物理变化 | |
| C. | 该反应元素的化合价没有发生改变 | |
| D. | 该反应中A、B、C都有可能是氧化物 |
4.在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:下列说法正确的是( )
| 物质 | A | B | C | D |
| 反应前质量/g | 4 | 6 | 111 | 4 |
| 反应后质量/g | 待测 | 15 | 0 | 84 |
| A. | 该反应中B和D两种物质的质量比为15:84 | |
| B. | 密闭容器中发生的化学反应属于化合反应 | |
| C. | 反应后密闭容器中A的质量为22g | |
| D. | 该反应中A、B、C、D四种物质的质量比为22:9:111:80 |
11.下列对分子、原子、离子的认识,正确的是( )
| A. | 分子是保持物质性质的最小粒子 | |
| B. | 原子是所有变化中最小的粒子,不可再分 | |
| C. | 原子是由分子构成的 | |
| D. | 氯化钠由钠离子和氯离子构成 |
1.经过了本学期的学习,我们知道了酸的一些性质.如图所示说明盐酸具有( )
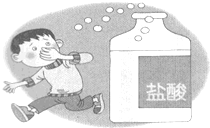

| A. | 酸性 | B. | 腐蚀性 | C. | 挥发性 | D. | 脱水性 |
8.2011年12月14日,我市举行了初中科学知识应用暨探究技能比赛.某校要求同学测定一颗从山上采集过来的石灰石中CaCO3的含量,根据自己的实验设计,小科取80克样品和足量的稀盐酸反应(所含杂质和稀盐酸不反应),测得反应后反应容器中物质的总质量(m)与反应时间(t)的关系如表:
请帮小明完成下列问题:
(1)当石灰石完全反应后,生成CO2的质量为22g.
(2)求该石灰石中CaCO3的质量分数,写出计算过程.
| 反应时间t∕s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 反应容器中物质的总质量(m)∕g | 280 | 275 | 270 | 266 | 262 | 258 | 258 |
(1)当石灰石完全反应后,生成CO2的质量为22g.
(2)求该石灰石中CaCO3的质量分数,写出计算过程.
