题目内容
通过晾晒海水或煮盐井水、盐湖水等,可以蒸发除去水分得到粗盐。粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等)。
[提出问题]如何才能将粗盐中难溶性杂质和可溶性杂质(氯化镁、氯化钙)除去,从而获得较纯的食盐晶体?
[资料准备]
|
20℃时,一些物质的溶解度 |
||
|
|
OH- |
CO32- |
|
Na+ |
溶 |
溶 |
|
Ca2+ |
微 |
不 |
|
Mg2+ |
不 |
微 |
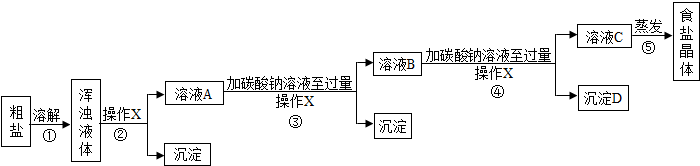
[实验方案]某同学为了提纯粗盐,设计了如下实验方案并进行实验。
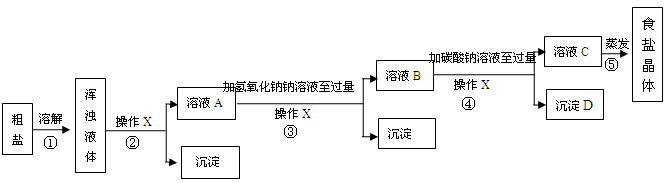
[交流与表达]
(1)实验步骤①和②的目的是 ;实验步骤③和④的目的是 。
(2)实验操作X的名称是 ,该操作中要用到的玻璃仪器有烧杯、玻璃棒和 。
(3)实验步骤③的主要目的是 (用化学方程式回答);判断氢氧化钠溶液已过量的方法是 。
(4)实验步骤④中生成的沉淀D是 。
(5)实验步骤⑤用蒸发溶剂的方法而不用降低溶液温度的方法获取食盐晶体,原因是 ;在蒸发食盐溶液的过程中要使用玻璃棒,作用是 。
[反思与评价]
(6)有同学认为只需要用氢氧化钠溶液和碳酸钠溶液中任意一种试剂就能将两种可溶性杂质出去,你认为这种方法 (选填“可行”或“不可行”),理由是 。
(7)有同学认为原实验方案不完善,做出这种评价的依据是 。
[实验方案设计]
(8)为了完善原实验发难,你设计的实验是 (仅写出补充部分的实验操作和现象)
(1)除去粗盐中的难溶性杂质(1分)
除去粗盐中的易溶性杂质CaCl2、MgCl2(1分)
(2)过滤(1分) 漏斗(1分)
(3)MgCl2+2NaOH====Mg(OH)2↓+2NaCl(1分) 不再继续产生沉淀
(4)碳酸钙(或CaCO3)(1分)
(5)氯化钠的溶解度收温度影响较小(1分)
搅拌溶液,避免因局部过热,造成液滴飞溅(1分)
(6)不可行(1分) MgCO3、Ca(OH)2均为微溶物,只用任意一种试剂就会有一种杂质生成微溶物而不能全部除去(1分)
(7)在除去MgCl2和CaCl2的同时,又引入了新的杂质NaOH和Na2CO3(或在除去Ca2+和Mg2+的同时又引入了新的杂质离子OH—和CO32—)(1分)
(8)向溶液C中逐滴加入稀盐酸至不再产生气泡为止(1分)
【解析】(1)浑浊液体经操作X分成了固体和液体,即操作X应该是将固体和液体进行分离的方法。所以操作X为过滤。过滤除去的是不溶于水的固体,因此实验步骤①和②是将粗盐中的不溶于水的固体除去。
粗盐中含有不溶性杂质和可溶性杂质(氯化镁、氯化钙)。实验步骤①和②是将粗盐中的不溶于水的固体(泥沙)除去。实验最后得到的是食盐晶体,所以实验步骤③和④除去的是粗盐中的可溶性杂质氯化镁、氯化钙。
(2)过滤操作中要用到的玻璃仪器有烧杯、玻璃棒和漏斗。
(3)氢氧化钠可与氯化镁、氯化钙中的氯化镁反应,生成氢氧化镁和氯化钠。反应的化学方程式为:MgCl2+2NaOH====Mg(OH)2↓+2NaCl
随着氢氧化钠的加入,会逐渐产生Mg(OH)2沉淀。当二者恰好完全反应时,氯化镁被完全除去。再加入氢氧化钠也不会产生沉淀。所以当不再继续产生沉淀时说明氢氧化钠已经过量。
(4)实验步骤④加入的碳酸钠会与氯化钙反应生成碳酸钙沉淀和氯化钠。
(5)氯化钠的溶解度受温度影响较小,不适合用降温结晶的方法。可用蒸发溶剂的方法得到氯化钠晶体。在蒸发食盐溶液的过程中,用玻璃棒搅拌是为了通过搅拌使溶液受热均匀,防止因局部液体过热造成液体向外溅出。
(6)如只使用碳酸钠溶液,则氯化镁会与之反应生成MgCO3。
只使用氢氧化钠溶液,则氯化钙会与之反应生成Ca(OH)2。
MgCO3、Ca(OH)2均为微溶物,无法全部除去,所以此方案不可行。
(7)因为步骤③和④分别使用了过量的氢氧化钠和碳酸钠,即二者有剩余,成为氯化钠中新的杂质。
(8)氢氧化钠和碳酸钠都可与盐酸反应生成氯化钠,所以为了除去溶液中存在的剩余的氢氧化钠和碳酸钠可加入适量的稀盐酸。当逐滴加入稀盐酸至不再产生气泡或溶液PH值为7时,两种杂质完全除去。
考点:粗盐的提纯、复分解反应
点评:本题综合性较强,结合粗盐的提纯考查了发生在酸碱盐之间的复分解反应。要求在推理实验过程时要细致认真。

 ,若X等于11,则该微粒表示
,若X等于11,则该微粒表示