题目内容
16.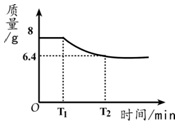 已知:CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.若8g CuO被CO完全反应,有关量的变化如下图,下列分析不正确的是( )
已知:CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.若8g CuO被CO完全反应,有关量的变化如下图,下列分析不正确的是( )| A. | 图中6.4表示生成Cu的质量 | B. | (8-6.4)表示消耗CO的质量 | ||
| C. | 生成CO2的质量为4.4 g | D. | T2时CuO反应完 |
分析 根据氧化铜的质量结合化学方程式可得剩余固体物质为铜,计算生成二氧化碳等的质量,进行分析;
解答 解:A、由方程式CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,可知CuO被CO完全反应,剩余固体质量为铜,铜的质量为6.4g,故正确;
B、由方程式CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,可知固体减少的质量(8-6.4)为氧化铜中的氧元素,而不是消耗CO的质量,故错误;
C、设生成CO2的质量为x
CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,
80 44
8g x
$\frac{80}{8g}=\frac{44}{x}$
x=4.4g,故正确;
D、T2时固体质量不在减少,说明反应已经停止,CuO反应完,故正确;
故选:B.
点评 本题考查了一氧化碳还原氧化铜的实验以及根据化学方程式的计算,完成此题,可以依据已有的知识结合反应的化学方程式进行.

练习册系列答案
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
6.下列变化中,属于化学变化的是( )
| A. | 酒精挥发 | B. | 葡萄酿酒 | C. | 车胎爆炸 | D. | 冰雪融化 |
7.缺少下列元素中,人体会患佝偻病的是( )
| A. | Fe | B. | Zn | C. | Na | D. | Ca |
4.下列物质属于氧化物的是( )
| A. | H2CO3 | B. | O3 | C. | C2H5OH | D. | SiO2 |
11.下列实验操作中,不正确的是( )
| A. |  滴加液体药品 | B. |  倾倒液体 | C. |  蒸发食盐水 | D. |  加热液体 |
8.在反应A+B═C+D中,4.4g B完全反应,生成10g C和1.8g d,若要生成20g C,则需要A的质量为( )
| A. | 8g | B. | 10g | C. | 14g | D. | 14.8g |
6.要想使一瓶接近饱和的石灰水变为饱和,具体操作有:①加入氢氧化钙;②升高温度;③降低温度;④加水;⑤蒸发水.其中措施正确的是( )
| A. | ①②④ | B. | ①③④ | C. | ①③⑤ | D. | ①②⑤ |