题目内容
已知:硝酸铵的化学式为NH4NO3,请根据硝酸铵的化学式计算:
(1)硝酸铵中,氮、氢、氧原子个数比为 .
(2)计算硝酸铵中各元素的质量比;
(3)计算硝酸铵中氮元素的质量分数;
(4)计算100kg硝酸铵中含有氮元素的质量.
(1)硝酸铵中,氮、氢、氧原子个数比为
(2)计算硝酸铵中各元素的质量比;
(3)计算硝酸铵中氮元素的质量分数;
(4)计算100kg硝酸铵中含有氮元素的质量.
考点:元素质量比的计算,元素的质量分数计算,化合物中某元素的质量计算
专题:化学式的计算
分析:(1)根据1个硝酸铵分子的构成进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中元素的质量分数=
×100%,进行分析解答.
(4)化合物中某元素的质量=该化合物的质量×该化合物中该元素的质量分数.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中元素的质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
(4)化合物中某元素的质量=该化合物的质量×该化合物中该元素的质量分数.
解答:解:(1)1个硝酸铵分子是由2个氮原子、4个氢原子和3个氧原子构成的,则硝酸铵分子中氮、氢、氧的原子个数比为2:4:3.故填:2:4:3;
(2)硝酸铵中氮、氢、氧三种元素的质量之比是(14×2):(1×4):(16×3)=7:1:12.故填:N:H:O=7:1:12;
(3)硝酸铵中氮元素的质量分数为
×100%=35%.故填:35%;
(4)100kg硝酸铵中含有氮元素的质量为:100kg×35%=35kg
答:100kg硝酸铵中含有氮元素的质量为35 kg.
故答案为:35kg.
(2)硝酸铵中氮、氢、氧三种元素的质量之比是(14×2):(1×4):(16×3)=7:1:12.故填:N:H:O=7:1:12;
(3)硝酸铵中氮元素的质量分数为
| 14×2 |
| 14×2+1×4+16×3 |
(4)100kg硝酸铵中含有氮元素的质量为:100kg×35%=35kg
答:100kg硝酸铵中含有氮元素的质量为35 kg.
故答案为:35kg.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
通过探究“我们吸入的空气和呼出气体有什么不同”这一问题,得出的结论正确的是( )
| A、我们吸入的气体全部是氧气 |
| B、我们呼出的气体全部是二氧化碳 |
| C、我们呼出的气体极易溶于水 |
| D、我们呼出的气体中二氧化碳含量较大 |
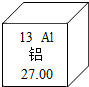 如图是元素周期表中的一格,从该图获取的信息是( )
如图是元素周期表中的一格,从该图获取的信息是( )| A、该元素的原子序数为27 |
| B、该元素的质子数为13 |
| C、该元素在地壳中的含量占第一位 |
| D、该元素属于非金属元素 |
下列变化,不属于缓慢氧化的是( )
| A、动植物的呼吸 |
| B、人体的新陈代谢 |
| C、食物的腐烂 |
| D、蜡烛的燃烧 |
科学家发明了一种以甲醇为原料的新型手机电池,手机待机时间可长达两个月,电池的反应原理为:2CH3OH+3X+4NaOH═2Na2CO3+6H2O,其中X的化学式为( )
| A、H2 |
| B、O2 |
| C、CO |
| D、CO2 |
空气是一种宝贵的自然资源.下列有关空气的说法正确的是( )
| A、空气中含量最多的气体是氧气 | ||
B、空气主要由氧气和氮气组成,其中氧气的质量约占空气质量的
| ||
| C、空气中分离出的氮气化学性质不活泼,可作食品保鲜的保护气 | ||
| D、空气质量报告中,空气质量级别数目越小,空气质量越差 |
下列有关空气成分的说法错误的是( )
| A、工业上以空气为原料,利用氮气和氧气的沸点不同分离出氧气 |
| B、航天工业上用氧气作反应原料,是因为氧气有可燃性 |
| C、空气中氮气的体积分数约为78% |
| D、空气中敞口放置的饼干变软是因为空气中含有水蒸气 |
分子、原子、离子都是构成物质的微粒,下列物质由阴、阳离子构成的是( )
| A、干冰 | B、水银 |
| C、金刚石 | D、氯化钠 |
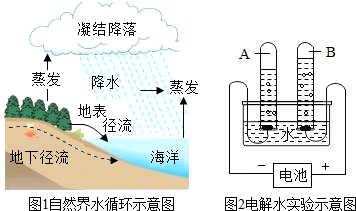 根据图1和图2回答下列问题.
根据图1和图2回答下列问题.