题目内容
元素周期表是我们学习和研究化学的重要工具,它的内容十分丰富.下面是元素周期表部分内容,请回答下列问题.
(1)6~11号元素中属于金属元素的有 (填元素符号).
(2)从表中可查出氧元素原子核内质子数是 ,根据氧原子的相对原子质量推断,氧原子核内的中子数是 .
(3)A元素在元素周期表中处于第三周期,则该元素原子核外有 电子层;如果A元素在元素周期表中处于ⅡA族,则该元素原子核外最外层有 个电子.
(4)氯元素原子的结构示意图是 ,它在化学变化中容易 (填“得”或“失”)电子,变成离子.
| 1 氢 H |
2 氦 He | |||||||
| 3 锂 Li |
4 铍 Be |
… | 5 硼 B |
6 碳 C |
7 氮 N |
8 氧 O |
9 氟 F |
10 氖 Ne |
| 11 钠 Na |
12 镁 Mg |
… | 13 铝 Al |
14 硅 Si |
15 磷 P |
16 硫 S |
17 氯 Cl |
18 氩 Ar |
(2)从表中可查出氧元素原子核内质子数是
(3)A元素在元素周期表中处于第三周期,则该元素原子核外有
(4)氯元素原子的结构示意图是
考点:元素周期表的特点及其应用,原子结构示意图与离子结构示意图
专题:化学用语和质量守恒定律
分析:(1)根据元素的名称解答;
(2)从元素周期表中氧元素的信息可解答;
(3)根据元素周期表中周期数与电子层数相同,主族数与最外层电子数相同来解答;
(4)根据氯元素质子数画出原子结构示意图.
(2)从元素周期表中氧元素的信息可解答;
(3)根据元素周期表中周期数与电子层数相同,主族数与最外层电子数相同来解答;
(4)根据氯元素质子数画出原子结构示意图.
解答:解:(1)6~11号元素中属于金属元素的有钠;
(2)从元素周期表中氧元素的信息可知氧元素原子核内质子数是8,相对原质量=质子数+中子数,氧原子的中子数=16-8=8;
(3)根据元素周期表中周期数与电子层数相同,第三周期的元素原子核外有3个电子数,主族数与最外层电子数相同,ⅡA族,则该元素原子核外最外层有2个电子;
(4)氯元素原子的结构示意图是 ;最外层电子数大于4的易得电子形成离子;
;最外层电子数大于4的易得电子形成离子;
答案:(1)Na;(2)8,8;(3)3个,2;(4)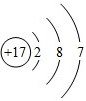 ,得.
,得.
(2)从元素周期表中氧元素的信息可知氧元素原子核内质子数是8,相对原质量=质子数+中子数,氧原子的中子数=16-8=8;
(3)根据元素周期表中周期数与电子层数相同,第三周期的元素原子核外有3个电子数,主族数与最外层电子数相同,ⅡA族,则该元素原子核外最外层有2个电子;
(4)氯元素原子的结构示意图是
 ;最外层电子数大于4的易得电子形成离子;
;最外层电子数大于4的易得电子形成离子;答案:(1)Na;(2)8,8;(3)3个,2;(4)
 ,得.
,得.点评:本题难度不大,考查学生对元素周期表知识的总结应用能力,掌握元素周期表中同一纵行的原子的特征(同一纵行,原子最外层电子数相同,从上到下电子层数逐渐增加)是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
用括号内试剂除去下列物质中的杂质,其中不正确的是( )
| A、氢氧化钠溶液混有的碳酸钠(石灰水) |
| B、硝酸铜溶液混有的硝酸银(铜粉) |
| C、二氧化碳中混有的氯化氢气体(氢氧化钠溶液) |
| D、氧气中混有的水蒸气(浓硫酸) |
化学中常常出现“1+1≠2”的有趣现象,但也有例外,下列符合“1+1=2”的事实是( )
| A、20℃,1L水与1L酒精混合后的体积等于2L |
| B、20℃,1g镁和1g稀硫酸充分反应后所得的溶液质量为2g |
| C、20℃,1g硫粉在1g氧气中完全燃烧后生成2g二氧化硫 |
| D、20℃,1个氢分子和1个氧分子充分反应生成2个水分子 |
 在利用高锰酸钾制取氧气的实验中,小明利用老师提供的以下实验仪器(序号A~E)
在利用高锰酸钾制取氧气的实验中,小明利用老师提供的以下实验仪器(序号A~E)