题目内容
20.下面是两种化肥标签的一部分,请回答: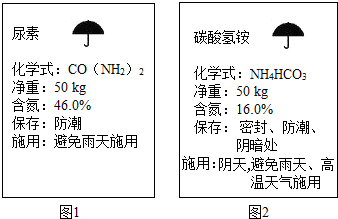
(1)从标签上看,这两种化肥属于氮肥(填 氮肥、磷肥、钾肥),碳酸氢铵不同于尿素的化学性质是碳酸氢铵高温易分解.
(2)这种“尿素”和“碳酸氢铵”的含氮的质量比为23:8.
(3)从含氮量角度,50kg这种碳酸氢铵相当于17.4kg(精确到0.1)这种尿素.
分析 (1)根据标签,碳酸氢铵避免高温施用,进行解答;
(2)根据“尿素”和“碳酸氢铵”的含氮的质量比即为标签上质量分数的比;进行解答;
(3)先求出50kg这种碳酸氢铵的含氮质量,除以这种尿素的含氮质量分数,即可解答.
解答 解:(1)尿素和碳酸氢铵都含有氮元素,属于氮肥;
根据标签,碳酸氢铵避免高温施用,可知碳酸氢铵不同于尿素的化学性质是碳酸氢铵高温易分解;
故答案为:氮肥;碳酸氢铵高温易分解.
(2)根据“尿素”和“碳酸氢铵”的含氮的质量比即为标签上质量分数的比;所以这种“尿素”和“碳酸氢铵”的含氮的质量比为:46%:16%=23:8;
故答案为:23:8;
(3)50kg这种碳酸氢铵的含氮质量为:50kg×16%=8kg,
相当于这种含氮尿素的质量为:8kg÷46%=17.4kg;
故答案为:17.4.
点评 本题考查学生根据物质的质量分数进行分析解题的能力.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
4. 汞使用的历史很悠久,用途很广泛.在元素周期表中,汞元素的信息如图所示,对图中信息解释正确的是( )
汞使用的历史很悠久,用途很广泛.在元素周期表中,汞元素的信息如图所示,对图中信息解释正确的是( )
 汞使用的历史很悠久,用途很广泛.在元素周期表中,汞元素的信息如图所示,对图中信息解释正确的是( )
汞使用的历史很悠久,用途很广泛.在元素周期表中,汞元素的信息如图所示,对图中信息解释正确的是( )| A. | 汞属于金属元素 | B. | 汞原子核外电子数是200.6 | ||
| C. | 汞原子核内中子数是80 | D. | 汞原子的相对原子质量是80 |
5.下列有关水的认识错误的是( )
| A. | 水是一种常见的溶剂 | B. | 自然界中的水过滤后变成纯水 | ||
| C. | 水的蒸馏是物理变化 | D. | 硬水和软水可用肥皂水鉴别 |
5.下列过程中主要发生化学变化的是( )
| A. |  洗发水洗去头发上的油污 | B. |  食醋除水垢 | ||
| C. | 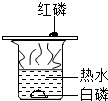 探究燃烧的条件 | D. |  黄豆磨制成豆浆 |
12.某同学在探究“酸与碱能否发生反应”时,用氢氧化钠的稀溶液、稀盐酸和酸碱指示剂进行实验的过程见如图.下图所加试剂①②③分别是( )
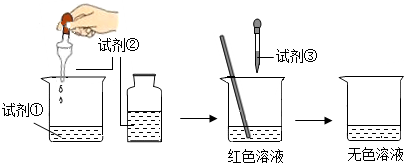

| A. | 稀NaOH溶液、石蕊溶液、稀盐酸 | B. | 稀盐酸、石蕊溶液、稀NaOH溶液 | ||
| C. | 稀盐酸、酚酞溶液、稀NaOH溶液 | D. | 稀NaOH溶液、酚酞溶液、稀盐酸 |
9. 实验室中有一瓶长期使用的氢氧化钠固体样品,某兴趣小组的同学对该样品的成分及含量进行探究.
实验室中有一瓶长期使用的氢氧化钠固体样品,某兴趣小组的同学对该样品的成分及含量进行探究.
发现问题】该样品中含有哪些物质?
【查阅资料】①NaOH在空气中不会转化成NaHCO3.
②BaCl2溶液呈中性,Ba(OH)2是可溶性碱
③CO2在饱和的NaHCO3溶液中几乎不溶解
【提出猜想】
猜想Ⅰ:NaOH
猜想Ⅱ:Na2CO3
猜想Ⅲ:NaOH和Na2CO3
【设计实验】
【收集证据】(1)若现象A是有气泡产生,则X溶液为稀盐酸,则猜想Ⅰ(填“猜想Ⅰ”、“猜想Ⅱ”或“猜想Ⅲ”)不成立.
(2)若X溶液为BaCl2溶液,现象A是有白色沉淀生成,则产生沉淀的化学方程式是BaCl2+Na2CO3═BaCO3↓+2NaCl,取反应后的上层清液,测定其PH,当PH>7(填“>”、“<”或“=”),则证明猜想Ⅲ成立.
【定量分析】确定部分变质样品中Na2CO3的质量分数.
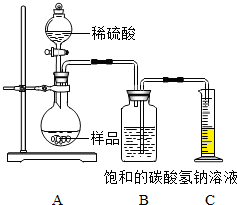
兴趣小组的同学用如图所示装置进行实验.
步骤如下:①按图连接好装置,并检查气密性;②准确称取该样品1.0g,放入烧瓶内;③打开活塞,滴加30.0%的稀硫酸至过量,关闭活塞;④反应结束后,量筒内液体的读数为55.0mL.(已知:室温条件下,CO2的密度为1.6g•L-1)
(1)B装置集气瓶内原有的空气对实验结果没有(填“有”或“没有”)影响.饱和NaHCO3溶液如果用水代替,则所测CO2体积偏小(填“偏大”、“偏小”或“不变”).
(2)计算该样品中Na2CO3的质量分数(写出计算过程,计算结果保留一位小数)
【实验反思】有同学指出,上述三种猜想并不全面,请再提出一种猜想NaOH、Na2CO3、H2O.
 实验室中有一瓶长期使用的氢氧化钠固体样品,某兴趣小组的同学对该样品的成分及含量进行探究.
实验室中有一瓶长期使用的氢氧化钠固体样品,某兴趣小组的同学对该样品的成分及含量进行探究.发现问题】该样品中含有哪些物质?
【查阅资料】①NaOH在空气中不会转化成NaHCO3.
②BaCl2溶液呈中性,Ba(OH)2是可溶性碱
③CO2在饱和的NaHCO3溶液中几乎不溶解
【提出猜想】
猜想Ⅰ:NaOH
猜想Ⅱ:Na2CO3
猜想Ⅲ:NaOH和Na2CO3
【设计实验】
| 实验操作 | 实验现象 |
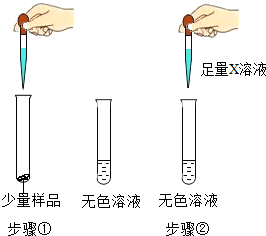 | 步骤①:样品全部溶解 步骤②:观察到现象A |
(2)若X溶液为BaCl2溶液,现象A是有白色沉淀生成,则产生沉淀的化学方程式是BaCl2+Na2CO3═BaCO3↓+2NaCl,取反应后的上层清液,测定其PH,当PH>7(填“>”、“<”或“=”),则证明猜想Ⅲ成立.
【定量分析】确定部分变质样品中Na2CO3的质量分数.
兴趣小组的同学用如图所示装置进行实验.
步骤如下:①按图连接好装置,并检查气密性;②准确称取该样品1.0g,放入烧瓶内;③打开活塞,滴加30.0%的稀硫酸至过量,关闭活塞;④反应结束后,量筒内液体的读数为55.0mL.(已知:室温条件下,CO2的密度为1.6g•L-1)
(1)B装置集气瓶内原有的空气对实验结果没有(填“有”或“没有”)影响.饱和NaHCO3溶液如果用水代替,则所测CO2体积偏小(填“偏大”、“偏小”或“不变”).
(2)计算该样品中Na2CO3的质量分数(写出计算过程,计算结果保留一位小数)
【实验反思】有同学指出,上述三种猜想并不全面,请再提出一种猜想NaOH、Na2CO3、H2O.
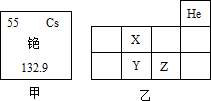 元素周期表是学习和研究化学的重要工具,试根据图示回答相应问题:
元素周期表是学习和研究化学的重要工具,试根据图示回答相应问题: