题目内容
19.稀硫酸、硫酸铜溶液都不能用铁制容器盛装,其原因是(用化学方程式表示)Fe+H2SO4=FeSO4+H2↑,Fe+CuSO4═FeSO4+Cu.分析 在金属活动性顺序中,氢前边的金属能与盐酸或硫酸反应生成了盐和氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,据此分析写出反应的化学方程式.
解答 解:由于在金属活动顺序表中,铁位于氢和铜的前边,铁能与稀硫酸和硫酸铜反应,所以,稀硫酸、硫酸铜溶液都不能用铁制容器盛装.反应的方程式分别是:Fe+H2SO4=FeSO4+H2↑,Fe+CuSO4═FeSO4+Cu.
故答为:Fe+H2SO4=FeSO4+H2↑,Fe+CuSO4═FeSO4+Cu.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
10.下列不属于中和反应在生产生活中的应用的是( )
| A. | 用石灰粉改良酸性土壤 | B. | 往造纸厂排放的碱溶液中加盐酸 | ||
| C. | 含氢氧化铝的胃药治疗盐酸过多 | D. | 硫酸铜与碱石灰配置波尔多液 |
7.一个碳原子的质量是1.993×10-26Kg,碳的相对原子质量为( )
| A. | 12g | B. | $\frac{1}{12}$ | ||
| C. | 12 | D. | $\frac{1.993×1{0}^{-26}Kg}{12}$ |
4.已知氯化铁溶液有如下性质:和铜反应生成氯化亚铁和氯化铜;和铁反应生成氯化亚铁.请根据上述信息完成有一包铁粉和铜粉混合物,为确定其组成将不同质量的样品分别放入FeCl3溶液中(其他用品略),实验数据记录如下
下列结论错误的是( )
| 组别 | ① | ② | ③ | ④ |
| 溶液中FeCl3的质量(g) | 65 | 65 | 65 | 65 |
| 混合粉末质量/g | 6 | 13.2 | 24 | 36 |
| 反应后剩余固体质量/g | 0 | 1.28 | 12.8 | 24.8 |
| A. | 第①组:反应后溶液中含有32.5克FeCl3 | |
| B. | 第②组:在反应后溶液中放入一根铁丝,铁钉表面无变化 | |
| C. | 第③组:剩余固体中滴加盐酸无气泡产生 | |
| D. | 第④组:剩余固体中铁与铜的物质的量之比为1:3 |
11.他们取样品125g,用35%的盐酸处理,其实验数据如下:
请回答下列问题
(1)该石灰石样品中含碳酸钙的质量分数是多少;
(2)实验过程中实际参加反应的盐酸的质量是多少,(精确到0.1g).
| 实验次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 加入稀盐酸体积/mL | 40 | 40 | 40 | 40 | 40 |
| 剩余固体的质量/g | 103 | 73 | 36 | 33 | 25 |
(1)该石灰石样品中含碳酸钙的质量分数是多少;
(2)实验过程中实际参加反应的盐酸的质量是多少,(精确到0.1g).
9.化学在生活中用途广泛,下列有关说法错误的是( )
| A. | 人被蚊虫叮咬后,蚊虫在人的皮肤内分泌出蚁酸,为减轻痛痒可以在皮肤上涂一些浓氯化钠溶液 | |
| B. | 香烟烟气中的CO会使血红蛋白携氧能力降低 | |
| C. | 稀盐酸、稀硫酸都可用于金属表面除锈 | |
| D. | 自行车的车架表面喷涂油漆可以防止生锈 |
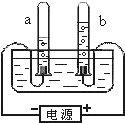 实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题:
实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题: