题目内容
高温煅烧100t含碳酸钙85%的石灰石至完全反应(假定杂质中不含钙元素、碳元素,也不发生任何变化),试用两种尽可能不同的方法求最后所得固体的质量.(已知碳酸钙在高温下分解生成氧化钙和二氧化碳)
考点:含杂质物质的化学反应的有关计算
专题:有关化学方程式的计算
分析:由石灰石的质量、碳酸钙的质量分数,根据赤铁矿炼铁的化学方程式可以列式计算出生成二氧化碳气体的质量或氧化钙的质量,进而可计算出最后所得固体的质量.
解答:解:设生成氧化钙气体的质量为x.
CaCO3
CaO+CO2↑
100 44
100t×85% x
=
x=37.4t
由最后所得固体的质量即为石灰石的质量与二氧化碳气体质量的差,其质量为100t-37.4t=63.6t
或设生成氧化钙的质量为y
CaCO3
CaO+CO2↑
100 56
100t×85% y
=
y=48.6t
则最后所得固体的质量(氧化钙的质量+杂质的质量)为48.6t+100t×(1-85%)=63.6t.
答:最后所得固体的质量为63.6t.
CaCO3
| ||
100 44
100t×85% x
| 100 |
| 44 |
| 100t×85% |
| x |
由最后所得固体的质量即为石灰石的质量与二氧化碳气体质量的差,其质量为100t-37.4t=63.6t
或设生成氧化钙的质量为y
CaCO3
| ||
100 56
100t×85% y
| 100 |
| 56 |
| 100t×85% |
| y |
则最后所得固体的质量(氧化钙的质量+杂质的质量)为48.6t+100t×(1-85%)=63.6t.
答:最后所得固体的质量为63.6t.
点评:本题难度不大,考查含杂质物质的化学方程式的计算,注意代入方程式计算的必须是纯物质的质量是正确解答此类题的关键.

练习册系列答案
相关题目
氧气是空气的主要成分之一.下列关于氧气的说法正确的是( )
| A、氧气能支持燃烧,可作燃料 |
| B、水中的生物能依靠微溶于水中的氧气而生存 |
| C、氧气对人们的生活百益无害 |
| D、带火星的木条一定能在含有氧气的集气瓶中复燃 |
下列关于溶液的说法中,正确的是( )
| A、溶液一定是无色透明的 |
| B、均一、稳定的液体一定是溶液 |
| C、饱和的氢氧化钠溶液中不能再溶解任何物质 |
| D、相同温度下,同种溶质在同种溶剂里的饱和溶液一定比不饱和溶液浓 |
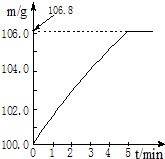 某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5g化肥样品与足量浓烧碱溶液加热,产生的氨气用100.0g废硫酸吸收.测得吸收氨气的溶液总质量m与反应时间t的变化如图所示.所涉及的反应为:(NH4)2SO4+2NaOH═Na2SO4+2H2O+2NH3↑;2NH3+H2SO4═(NH4)2SO4.请计算:
某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5g化肥样品与足量浓烧碱溶液加热,产生的氨气用100.0g废硫酸吸收.测得吸收氨气的溶液总质量m与反应时间t的变化如图所示.所涉及的反应为:(NH4)2SO4+2NaOH═Na2SO4+2H2O+2NH3↑;2NH3+H2SO4═(NH4)2SO4.请计算:
 如图是元素周期表中的一种元素,下列有关该元素的信息正确的是
如图是元素周期表中的一种元素,下列有关该元素的信息正确的是