题目内容
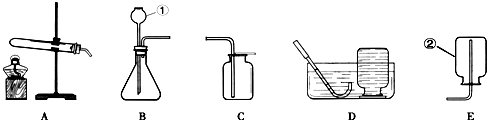
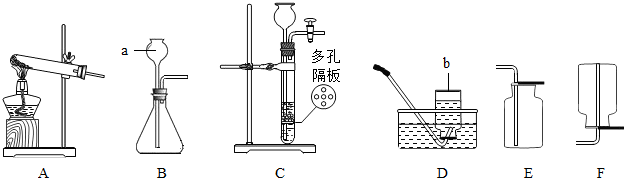
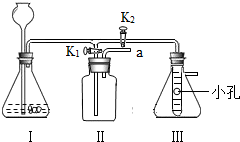
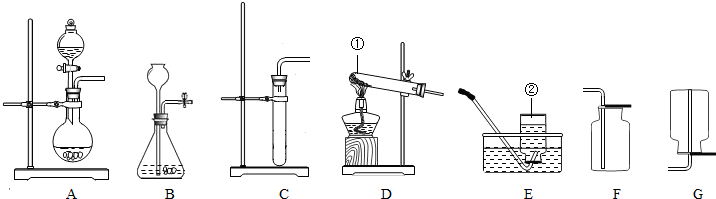
如图是实验室制取气体的一些装置,据图回答有关问题.(友情提示:以下所选装置均填装置序号)

(1)写出指定仪器的名称:①______;②______;
(2)实验室要用过氧化氢溶液和二氧化锰混合制氧气,若用A装置作氧气的发生装置,注射器中应放入的物质是______,锥形瓶中应放人的物质是______.该反应的化学方程式为______.用A作发生装置,比起B装置具有的主要优点是______.
(3)若实验室要用氯酸钾和二氧化锰混合为原料用装置C制氧气,该反应的化学方程式为______.该装置中试管口略向下倾斜的原因是______;要收集一瓶干燥的氧气,应选择装置______(填字母).
(4)实验室在常温下用块状固体电石与水反应制取乙炔气体,该反应必须严格控制加水速率,以免剧烈反应放热引起发生装置炸裂.你认为上图中最适合制取乙炔气体的发生装置是______.
解:(1)图中①是试管,②是用于加热的酒精灯;
故答案为:试管;酒精灯;
(2)若用A装置作氧气的发生装置,注射器中应放入的物质是液体过氧化氢溶液,则锥形瓶中放的是二氧化锰;过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的方程式是:2H2O2 2H2O2+O2↑;比较A、B装置可以看出:A具有可以控制液体的滴加速率,随时控制反应的发生和停止等优点;
2H2O2+O2↑;比较A、B装置可以看出:A具有可以控制液体的滴加速率,随时控制反应的发生和停止等优点;
故答案为:过氧化氢溶液;二氧化锰;2H2O2 2H2O2+O2↑;可以控制液体的滴加速率(合理均可);
2H2O2+O2↑;可以控制液体的滴加速率(合理均可);
(3)氯酸钾在二氧化锰作催化剂、加热的条件下生成氯化钾和氧气,反应方程式是:2KClO3 2KCl+3O2↑;加热固体药品时试管口都应向下倾斜,防止药品有潮气,加热时形成的冷凝水倒流入试管底部引起试管炸裂;氧气的密度比空气大,所以要收集一瓶干燥的氧气用向上排空气法;
2KCl+3O2↑;加热固体药品时试管口都应向下倾斜,防止药品有潮气,加热时形成的冷凝水倒流入试管底部引起试管炸裂;氧气的密度比空气大,所以要收集一瓶干燥的氧气用向上排空气法;
故答案为:2KClO3 2KCl+3O2↑;防止冷凝水倒流,使试管炸裂;E;
2KCl+3O2↑;防止冷凝水倒流,使试管炸裂;E;
(4)实验室在常温下用块状固体电石与水反应制取乙炔气体,可选择A或B作发生装置;该反应必须严格控制加水速率,以免剧烈反应放热引起发生装置炸裂,而A装置可以控制加水速率,进而可以控制反应速率,B不可以,所以选择A装置;
故答案为:A.
分析:(1)熟悉常见仪器,了解名称;
(2)根据装置特点和药品的状态分析判断;并依据过氧化氢分解的反应原理书写方程式;比较A、B装置可以看出:A具有可以控制液体的滴加速率,控制反应的发生和停止等优点;
(3)依据氯酸钾制取氧气的反应原理书写方程式;装置中试管口略向下倾斜的原因是:防止冷凝水倒流,使试管炸裂;收集干燥的气体用排空气法,并结合氧气的性质分析判断;
(4)根据电石与水反应的特点并结合上述装置分析判断.
点评:解答本题既要掌握实验室制取氧气的反应方程式、实验仪器、注意事项等知识,还要掌握装置的选取方法,并会结合题目要求灵活应用.
故答案为:试管;酒精灯;
(2)若用A装置作氧气的发生装置,注射器中应放入的物质是液体过氧化氢溶液,则锥形瓶中放的是二氧化锰;过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的方程式是:2H2O2
 2H2O2+O2↑;比较A、B装置可以看出:A具有可以控制液体的滴加速率,随时控制反应的发生和停止等优点;
2H2O2+O2↑;比较A、B装置可以看出:A具有可以控制液体的滴加速率,随时控制反应的发生和停止等优点;故答案为:过氧化氢溶液;二氧化锰;2H2O2
 2H2O2+O2↑;可以控制液体的滴加速率(合理均可);
2H2O2+O2↑;可以控制液体的滴加速率(合理均可);(3)氯酸钾在二氧化锰作催化剂、加热的条件下生成氯化钾和氧气,反应方程式是:2KClO3
 2KCl+3O2↑;加热固体药品时试管口都应向下倾斜,防止药品有潮气,加热时形成的冷凝水倒流入试管底部引起试管炸裂;氧气的密度比空气大,所以要收集一瓶干燥的氧气用向上排空气法;
2KCl+3O2↑;加热固体药品时试管口都应向下倾斜,防止药品有潮气,加热时形成的冷凝水倒流入试管底部引起试管炸裂;氧气的密度比空气大,所以要收集一瓶干燥的氧气用向上排空气法;故答案为:2KClO3
 2KCl+3O2↑;防止冷凝水倒流,使试管炸裂;E;
2KCl+3O2↑;防止冷凝水倒流,使试管炸裂;E;(4)实验室在常温下用块状固体电石与水反应制取乙炔气体,可选择A或B作发生装置;该反应必须严格控制加水速率,以免剧烈反应放热引起发生装置炸裂,而A装置可以控制加水速率,进而可以控制反应速率,B不可以,所以选择A装置;
故答案为:A.
分析:(1)熟悉常见仪器,了解名称;
(2)根据装置特点和药品的状态分析判断;并依据过氧化氢分解的反应原理书写方程式;比较A、B装置可以看出:A具有可以控制液体的滴加速率,控制反应的发生和停止等优点;
(3)依据氯酸钾制取氧气的反应原理书写方程式;装置中试管口略向下倾斜的原因是:防止冷凝水倒流,使试管炸裂;收集干燥的气体用排空气法,并结合氧气的性质分析判断;
(4)根据电石与水反应的特点并结合上述装置分析判断.
点评:解答本题既要掌握实验室制取氧气的反应方程式、实验仪器、注意事项等知识,还要掌握装置的选取方法,并会结合题目要求灵活应用.

练习册系列答案
相关题目