题目内容
在一次化学实验中,某小组的同学将稀盐酸滴入紫色石蕊溶液中,发现紫色石蕊溶液变红,他们欲对稀盐酸中哪种成分使紫色石蕊溶液变红进行探究:
【提出问题】究竟稀盐酸中哪种成分使紫色石蕊溶液变红?
【查阅资料】HCL在水中能够全部解离成H+和Cl-
【猜想假设】小明认为:可能是H2O使紫色石蕊溶液变红;
小华认为:可能是Cl-使紫色石蕊溶液变红;
小桐认为:可能是 (填化学符号)使紫色石蕊溶液变红
经过讨论,大家一致认为 的猜想不合理,理由是
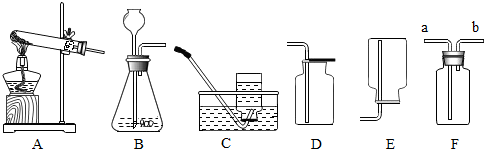
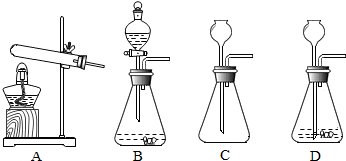
【实验探究】
【实验结论】大家经过实验分析得出的结论是稀盐酸中的H+能使紫色石蕊溶液变红
【拓展应用】试验后的溶液不能直接倒入下水管道,同学们想通过加入熟石灰的方法改变溶液的酸碱性,以达到直接排放的要求,请写出反应的化学方程式 (写出一个即可)
【提出问题】究竟稀盐酸中哪种成分使紫色石蕊溶液变红?
【查阅资料】HCL在水中能够全部解离成H+和Cl-
【猜想假设】小明认为:可能是H2O使紫色石蕊溶液变红;
小华认为:可能是Cl-使紫色石蕊溶液变红;
小桐认为:可能是
经过讨论,大家一致认为
【实验探究】
| 实验操作 | 实验现象 | 结论 |
| 向 | 无明显现象 | CL-不能使紫色石蕊溶液变红 |
| 向硫酸溶液中滴入紫色石蕊溶液 | 紫色石蕊溶液变红 |
【拓展应用】试验后的溶液不能直接倒入下水管道,同学们想通过加入熟石灰的方法改变溶液的酸碱性,以达到直接排放的要求,请写出反应的化学方程式
考点:实验探究物质的性质或变化规律,酸的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:可能是稀盐酸中的氢离子使石蕊试液变红色,每个氢离子带1个单位正电荷;
石蕊试液中含有水;
氯化钠溶液中含有氯离子;
稀硫酸中含有氢离子和硫酸根离子;
氢氧化钙和稀盐酸反应生成氯化钙和水,和稀硫酸反应生成硫酸钙和水.
石蕊试液中含有水;
氯化钠溶液中含有氯离子;
稀硫酸中含有氢离子和硫酸根离子;
氢氧化钙和稀盐酸反应生成氯化钙和水,和稀硫酸反应生成硫酸钙和水.
解答:解:【猜想假设】
小桐认为:可能是H+使紫色石蕊溶液变红;
经过讨论,大家一致认为小明的猜想不合理,理由是紫色石蕊溶液中含有水,如果水能使石蕊试液变红色,那么石蕊试液本身就是红色溶液.
故填:H+;小明;紫色石蕊溶液中含有水.
【实验探究】
向氯化钠溶液中滴入紫色石蕊溶液,无明显现象,说明CL-不能使紫色石蕊溶液变红;
向硫酸溶液中滴入紫色石蕊溶液,紫色石蕊溶液变红,说明H+能使紫色石蕊溶液变红.
故填:氯化钠溶液;H+能使紫色石蕊溶液变红.
【拓展应用】
氢氧化钙和稀盐酸或稀硫酸反应的化学方程式为:Ca(OH)2+2HCl═CaCl2+2H2O,或Ca(OH)2+H2SO4═CaSO4+2H2O.
故填:Ca(OH)2+2HCl═CaCl2+2H2O,或Ca(OH)2+H2SO4═CaSO4+2H2O.
小桐认为:可能是H+使紫色石蕊溶液变红;
经过讨论,大家一致认为小明的猜想不合理,理由是紫色石蕊溶液中含有水,如果水能使石蕊试液变红色,那么石蕊试液本身就是红色溶液.
故填:H+;小明;紫色石蕊溶液中含有水.
【实验探究】
向氯化钠溶液中滴入紫色石蕊溶液,无明显现象,说明CL-不能使紫色石蕊溶液变红;
向硫酸溶液中滴入紫色石蕊溶液,紫色石蕊溶液变红,说明H+能使紫色石蕊溶液变红.
故填:氯化钠溶液;H+能使紫色石蕊溶液变红.
【拓展应用】
氢氧化钙和稀盐酸或稀硫酸反应的化学方程式为:Ca(OH)2+2HCl═CaCl2+2H2O,或Ca(OH)2+H2SO4═CaSO4+2H2O.
故填:Ca(OH)2+2HCl═CaCl2+2H2O,或Ca(OH)2+H2SO4═CaSO4+2H2O.
点评:合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
下列关于化肥和农药的说法错误的是( )
| A、铵态氮肥应该避免与草木灰混用 |
| B、碳酸氢铵保存时应该避免高温和阳光照射 |
| C、农药本身有毒,应该禁止施用 |
| D、目前施用仍是最重要的作物保护手段 |
下列做法不存在事故隐患的是( )
| A、将白磷长期浸泡水中 |
| B、将燃气热水器安装在卫生间内 |
| C、向阴沟倾倒液化气燃烧废液 |
| D、存有大量熟石灰的露天石灰池附近未做标志 |
2014年世界环境日中国主题为“向污染宣战”.下列做法不符合这一主题的是( )
| A、用风能与太阳能替代燃煤发电 |
| B、提倡步行、骑自行车等“低碳”出行方式 |
| C、施用大量的化肥和农药以提高农作物产量 |
| D、淘汰污染严重的黄标车和污染严重的老式锅炉 |

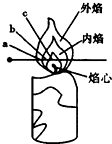 化学兴趣小组的三位同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.
化学兴趣小组的三位同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.