题目内容
5.用一种试剂就能鉴别稀盐酸、氢氧化钠溶液、氯化钠溶液的是 ( )| A. | BaCl2 溶液 | B. | 石蕊试液 | C. | AgNO3溶液 | D. | 酚酞试液 |
分析 根据三种物质与同种试剂反应产生的不同现象来鉴别它们,若两种物质与同种物质反应的现象相同,则无法鉴别它们.
解答 解:A、BaCl2 溶液与稀盐酸、氢氧化钠溶液、氯化钠溶液均不反应,不能出现三种明显不同的现象,不能鉴别,故选项错误.
B、紫色石蕊溶液遇酸性溶液变红,遇碱性溶液变蓝,稀盐酸、氢氧化钠溶液、氯化钠溶液分别显酸性、碱性、中性,使石蕊溶液分别显示红色、蓝色、紫色,能出现三种明显不同的现象,可以鉴别,故选项正确.
C、稀盐酸、氯化钠溶液均能与AgNO3溶液反应生成氯化银白色沉淀,不能出现三种明显不同的现象,不能鉴别,故选项错误.
D、无色酚酞溶液遇酸性溶液不变色,遇碱性溶液变红色,稀盐酸、氢氧化钠溶液、氯化钠溶液分别显酸性、碱性、中性,使酚酞溶液分别显示无色、红色、无色,不能出现三种明显不同的现象,不能鉴别,故选项错误.
故选:B.
点评 本题有一定难度,在解决鉴别物质题时,判断的依据是:所选试剂需要与待鉴别的物质反应并出现明显不同的现象.

练习册系列答案
相关题目
16. 如表是KNO3、NaCl在不同温度下的部分溶解度数据,请回答问题:
如表是KNO3、NaCl在不同温度下的部分溶解度数据,请回答问题:
(1)10℃时,KNO3溶解度是20.9g.
(2)40℃时,将70gKNO3固体加入100g水中,充分搅拌,形成的溶液质量为163.9g.
(3)60℃时,KNO3的饱和溶液中含有少量NaCl,通过降温结晶方法获得较纯净的KNO3晶体.
(4)t℃时,NaCl和KNO3的饱和溶液溶质质量分数相同,该温度范围是b.
a.10℃~20℃b.20℃~40℃c.40℃~60℃d.60℃~80℃
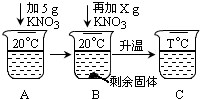
(5)向20mL水中溶解一定量KNO3固体的操作如图:请根据实验现象和溶解度数据回答:A、B、C中溶液一定不饱和溶液的是A.当x=1.32g时,B中恰好没有固体剩余.
 如表是KNO3、NaCl在不同温度下的部分溶解度数据,请回答问题:
如表是KNO3、NaCl在不同温度下的部分溶解度数据,请回答问题:| 温度(℃) | 10 | 20 | 40 | 60 | 80 |
| KNO3 | 20.9 | 31.6 | 63.9 | 110 | 169 |
| NaCl | 35.8 | 36 | 36.6 | 37.3 | 38.4 |
(2)40℃时,将70gKNO3固体加入100g水中,充分搅拌,形成的溶液质量为163.9g.
(3)60℃时,KNO3的饱和溶液中含有少量NaCl,通过降温结晶方法获得较纯净的KNO3晶体.
(4)t℃时,NaCl和KNO3的饱和溶液溶质质量分数相同,该温度范围是b.
a.10℃~20℃b.20℃~40℃c.40℃~60℃d.60℃~80℃
(5)向20mL水中溶解一定量KNO3固体的操作如图:请根据实验现象和溶解度数据回答:A、B、C中溶液一定不饱和溶液的是A.当x=1.32g时,B中恰好没有固体剩余.
13.某同学欲测定一瓶标签残缺的硫酸镁溶液的溶质质量分数,取60g该溶液于烧杯中,向其中滴入足量的氢氧化钠溶液,记录有关数据如表:
反应的化学方程式为:MgSO4+2NaOH═Na2SO4+Mg(OH)2
(1)反应生成氢氧化镁沉淀的质量为2.9g;
(2)计算MgSO4溶液中溶质的质量分数10%(根据化学方程式计算);
(3)100g溶质质量分数为10%的NaOH溶液中氧元素的质量为84g.
| 反应前 | 反应后 | |
| 烧杯和硫酸镁溶液的质量 | 溶质质量分数为10%的NaOH溶液 | 过滤后烧杯和溶液总质量 |
| 80g | 100g | 177.1g |
(1)反应生成氢氧化镁沉淀的质量为2.9g;
(2)计算MgSO4溶液中溶质的质量分数10%(根据化学方程式计算);
(3)100g溶质质量分数为10%的NaOH溶液中氧元素的质量为84g.
20.某同学在一次化学实验中,不慎将盐酸滴到大理石的地面上,他看见地面上有气泡产生,该气体是 ( )
| A. | 氧气 | B. | 氢气 | C. | 二氧化碳 | D. | 二氧化硫 |
17.菱镁矿的主要成分是MgCO3,为了分析某菱镁矿中镁元素的含量,某学习小组进行了实验研究.取10g菱镁矿,逐渐加入未知浓度的H2SO4溶液,生成的气体全部用NaOH溶液吸收,NaOH溶液增加的质量记录如表:
说明:菱镁矿中的杂质不溶于水,不与酸发生反应.
(1)菱镁矿中MgCO3的质量分数为84%.
(2)10g菱镁矿与100克H2SO4溶液恰好完全反应,请计算所得溶液中溶质的质量分数.(写出计算过程,结果保留至0.1%)
| 加入H2S04溶液的质量/g | 50 | 100 | 150 | 200 |
| NaOH溶液增加的质量/g | 2.2 | 4.4 | 4.4 | 4.4 |
(1)菱镁矿中MgCO3的质量分数为84%.
(2)10g菱镁矿与100克H2SO4溶液恰好完全反应,请计算所得溶液中溶质的质量分数.(写出计算过程,结果保留至0.1%)