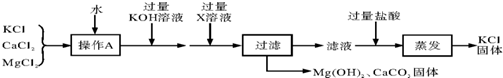
题目内容
17. 向53g质量分数为10%的碳酸钠溶液中逐滴加入质量分数为5%的稀盐酸,生成二氧化碳的质量随加入盐酸质量的变化关系如图所示.(不考虑CO2的溶解)
向53g质量分数为10%的碳酸钠溶液中逐滴加入质量分数为5%的稀盐酸,生成二氧化碳的质量随加入盐酸质量的变化关系如图所示.(不考虑CO2的溶解)已知:
OB段反应的化学方程式为Na2CO3+HCl═NaCl+NaH CO3
BD段(不含B点)反应的化学方程式为NaH CO3+HCl═NaCl+H2O+CO2↑
请回答:
(1)53g质量分数为10%的碳酸钠溶液中溶质质量为5.3g.
(2)A点对应溶液中溶质有Na2CO3、NaCl、NaHCO3(填化学式).
(3)B点横坐标为.36.5(计算结果保留1位小数,下同)
(4)假设C点横坐标为54.75,计算C点对应的二氧化碳质量.(写出计算过程)
分析 (1)根据溶质的质量分数计算;
(2)根据生成二氧化碳的质量随加入盐酸质量的变化关系分析A点对应溶液中溶质;
(3)根据在B点时Na2CO3与盐酸恰好反应生成了氯化钠和碳酸氢钠计算分析;
(4)根据碳酸氢钠与盐酸反应的方程式及参加该反应盐酸的质量计算C点对应的二氧化碳质量.
解答 解:(1)53g质量分数为10%的碳酸钠溶液中溶质质量为:53g×10%=5.3g.
(2)由生成二氧化碳的质量随加入盐酸质量的变化关系可知,在如图A点时,溶液中碳酸钠部分与盐酸反应生成了氯化钠和碳酸氢钠,所以,对应溶液中溶质有:Na2CO3、NaCl、NaHCO3.
(3)由生成二氧化碳的质量随加入盐酸质量的变化关系可知,在如图B点时,溶液中碳酸钠恰好与盐酸反应生成了氯化钠和碳酸氢钠,
设与碳酸钠反应生成了氯化钠和碳酸氢钠的盐酸的质量为x
Na2CO3+HCl═NaCl+NaH CO3
106 36.5
5.3g x×5%
$\frac{106}{36.5}=\frac{5.3g}{x×5%}$ 解得x=36.5g
(4)设C点对应的二氧化碳质量为y.
NaHCO3+HCl═NaCl+H2O+CO2↑
36.5 44
(54.75g-36.5g)×5% y
$\frac{36.5}{44}=\frac{(54.75g-36.5g)×5%}{y}$ 解得:y=1.1g
故答为:(1)5.3;(2)Na2CO3、NaCl、NaH CO3;(3)36.5;(4)C点对应的二氧化碳质量未1.1g.
点评 难度较大,考查了利用图形结合化学方程式对问题进行分析和计算的能力.

练习册系列答案
相关题目
7.如图为初中化学常见气体的发生、收集装置.有关这些装置的说法不正确的是( )


| A. | 装置Ⅰ可作为加热固体制取气体的发生装置 | |
| B. | 装置Ⅱ可用于制取二氧化碳气体,不可以用于制取氧气 | |
| C. | 装置Ⅲ、Ⅳ可用于收集密度与空气密度差距较大,且不与空气中各成分反应的无毒气体 | |
| D. | 装置Ⅳ、Ⅴ都可用于实验室收集氧气 |
8.向一定质量的AgNO3和Fe(NO3)2的混合溶液中加入m克Zn粉,充分反应后过滤,将滤渣洗涤、干燥后称量,得到的固体质量为m克.据此,下列说法不正确的是( )
| A. | 滤渣中的物质至少有两种 | |
| B. | 取反应后的滤液滴加稀盐酸,有白色沉淀产生 | |
| C. | 取滤渣滴加稀盐酸,一定有气泡产生 | |
| D. | 取反应后的滤液观察,滤液可能呈浅绿色 |
5.下列有关实验操作“先”与“后”的说法中正确的是( )
| A. | 测定溶液的PH,先将试纸用水湿润,后用干净的玻璃棒蘸取待测液点在试纸上 | |
| B. | 加热氯酸钾制取氧气时,用排水法收集气体;实验完毕后,先熄灭酒精灯,后将导管从水槽中移出 | |
| C. | 一氧化碳还原氧化铁时,先加热氧化铁粉末至红热,后通入一氧化碳气体 | |
| D. | 稀释浓硫酸时,先在烧杯中倒入水,后将浓硫酸沿烧杯壁缓慢地注入水中,并不断搅拌 |
12. 甲、乙、丙三种固体物质的溶解度曲线如图所示,下列分析错误的是( )
甲、乙、丙三种固体物质的溶解度曲线如图所示,下列分析错误的是( )
 甲、乙、丙三种固体物质的溶解度曲线如图所示,下列分析错误的是( )
甲、乙、丙三种固体物质的溶解度曲线如图所示,下列分析错误的是( )| A. | t1℃时,甲、乙、丙三种物质的溶解度大小关系是 丙>乙>甲 | |
| B. | 含有甲、乙、丙三种物质的混合溶液恒温蒸发时首先析出乙,说明在此温度下乙的溶解度最小 | |
| C. | 将t3℃时,甲、乙、丙三种物质的饱和溶液降温至t2℃,所得溶液的质量分数关系是丙>甲=乙 | |
| D. | 若固体甲中混有少量乙,可采用降温结晶法提纯甲 |
5.蔓延全球的甲流疫情,使一些不法商人借机炒作大蒜,使其价格疯涨的甚至比肉还贵--“蒜你狠”一度成为时下流行的网络语.大蒜中含有大蒜素(化学式为C6H10S2),下列关于大蒜素说法不正确的是( )
| A. | 大蒜素属于有机物 | |
| B. | 大蒜素由碳、氢、硫三种元素组成 | |
| C. | 大蒜素中碳氢硫的原子个数比为3:5:1 | |
| D. | 1个大蒜素分子是由6个碳原子、5个氢分子和2个硫原子构成的 |
12.下列实验操作中,正确的是( )
| A. | 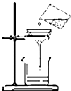 过滤 | B. |  量取液体 | C. | 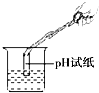 测定溶液的pH | D. | 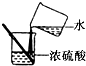 浓硫酸的稀释 |
10.为了探究“铁、铜、锌金属性强弱”,某学习小组设计了下列四个实验方案,其中不合理的( )
| A. | 分别将Zn和Cu加入到FeCl2溶液中 | B. | 分别将Fe和Cu加入到ZnSO4溶液中 | ||
| C. | 将Fe分别加入ZnSO4和CuSO4溶液中 | D. | 分别把Fe、Cu、Zn加入到稀盐酸中 |